
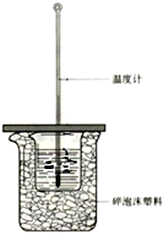
 50mL0.50mol/L鹽酸與50mL0.55mol/LNaOH溶液在如圖上所示的裝置中進行中和反應.通過測定反應過程中所放出的熱量可計算中和熱.
50mL0.50mol/L鹽酸與50mL0.55mol/LNaOH溶液在如圖上所示的裝置中進行中和反應.通過測定反應過程中所放出的熱量可計算中和熱.分析 (1)根據量熱計的構造來判斷該裝置的缺少儀器;
(2)中和熱測定實驗成敗的關鍵是保溫工作;
(3)不蓋硬紙板,會有一部分熱量散失;
(4)為了保證酸全部反應,堿要稍過量;
(5)弱電解質電離吸熱.
解答 解:(1)根據量熱計的構造可知該裝置的缺少儀器是環形玻璃攪拌棒;
故答案為:環形玻璃攪拌棒;
(2)中和熱測定實驗成敗的關鍵是保溫工作,大小燒杯之間填滿碎紙條的作用是:減少實驗過程中的熱量損失;
故答案為:減少實驗過程中的熱量損失;
(3)大燒杯上如不蓋硬紙板,會有一部分熱量散失,求得的中和熱數值將會減小;
故答案為:偏小;
(4)NaOH的濃度大于HCl的濃度,使鹽酸完全被中和,減少了鹽酸揮發對實驗的影響;
故答案為:保證鹽酸完全被中和;
(5)一水合氨為弱堿,電離過程為吸熱過程,所以用氨水代替NaOH溶液反應,反應放出的熱量偏小,中和熱的數值偏小;
故答案為:偏小.
點評 本題考查學生有關中和熱的測定,題目難度中等,注意理解中和熱的概念和測定原理是解題的關鍵.


科目:高中化學 來源: 題型:解答題
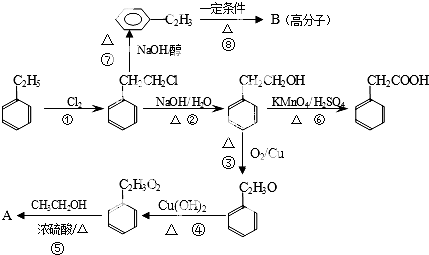
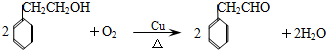
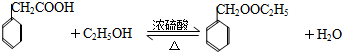

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 與漂白粉溶液反應的離子方程式:Ca2++SO32-═CaSO3↓ | |
| B. | 通入SO2至過量:c(Na+)=2[c(SO32-)+c(HSO3-)+c(H2SO3)] | |
| C. | 通入HCl至溶液pH=7:c(HSO3-)<c(Cl-) | |
| D. | 加入NaOH固體可使溶液中水的電離程度增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O | |
| B. | 用FeCl3溶液腐蝕銅來制作印刷電路板:2Fe3++Cu═2Fe2++Cu2+ | |
| C. | 向Na2SiO3溶液中通入過量SO2:SiO32-+SO2+H2O═H2SiO3↓+SO32- | |
| D. | 向Al (SO4)3溶液中加入過量的NH3•H2O:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用S制備H2SO4 | B. | 用CaCO3、Na2CO3、SiO2生產玻璃 | ||
| C. | 將海水中的MgSO4轉變為金屬Mg | D. | 用NO2生產HNO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金屬性最強的是銫 | |
| B. | 密度隨核電荷數的增加而增大 | |
| C. | 單質的熔、沸點隨核電荷數的增加而降低 | |
| D. | 最高價氧化物的水化物的堿性隨核電荷數的增加而增強 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將pH=6的H2SO4 稀釋1000倍后,c(H+)=2 c(SO42-) | |
| B. | 0.1 mol L-1的 Na2CO3溶液中:c(OH- )=c(HCO3- )+c(H+)+c(H2CO3) | |
| C. | 濃度均為0.1 mol L-1的 NaClO 溶液和 CH3COONa 溶液中,c(ClO-)<c(CH3COO-) | |
| D. | 濃度分別為0.1 mol L-1和0.01 mol L-1的CH3COOH溶液中:c(CH3COO-)前者是后者的10倍 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com