
| A. | 標準狀況下5.6L 氫氣 | B. | 6.02×1022個H2SO4 | ||
| C. | 11gCO2 | D. | 4℃時9mL水 |
分析 A、根據n=$\frac{V}{{V}_{m}}$計算氫氣的物質的量;
B、根據n=$\frac{N}{{N}_{A}}$;
C、根據n=$\frac{m}{M}$;
D、根據m=ρV計算水的質量,再根據n=$\frac{m}{M}$計算水的物質的量;結合分子含有原子數目計算含有原子總物質的量,據此判斷.
解答 解:A、標況下,5.6L氫氣的物質的量為$\frac{5.6L}{22.4L/mol}$=0.25mol,所以原子總物質的量為0.5mol;
B、6.02×1022個H2SO4的物質的量為0.1mol,所以原子總物質的量為0.7mol;
C、11gCO2的物質的量為0.25mol,所以原子總物質的量為0.75mol;
D、9mL水的質量為9g,其物質的量為0.5mol,含有原子為0.5mol×3=1.5mol;
所以4℃時9mL水所含原子總數最多,
故選D.
點評 本題考查物質的量有關計算,注意微粒數目的計算的方法,比較基礎,難度中等.


 金牌教輔培優優選卷期末沖刺100分系列答案
金牌教輔培優優選卷期末沖刺100分系列答案科目:高中化學 來源: 題型:解答題
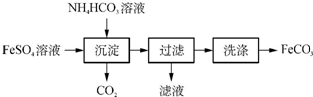
| 實驗步驟 | 實驗操作步驟 |
| Ⅰ | 取一定質量的FeCO3固體置于坩堝中,高溫煅燒至質量不再減輕,冷卻至室溫 |
| Ⅱ | 取少量實驗步驟Ⅰ所得固體置于一潔凈的試管中,用足量的稀硫酸溶解 |
| Ⅲ | 向實驗步驟Ⅱ所得溶液中滴加KSCN溶液,溶液變紅 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 甲組同學擬用高錳酸鉀制取氧氣,并收集和測量氧氣體積,其裝置如圖所示.
甲組同學擬用高錳酸鉀制取氧氣,并收集和測量氧氣體積,其裝置如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
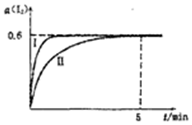 將1.0mol I2 (g)和2.4mcl H2置于某2L密閉容器中,在某一溫度下發生反應H2(g)+I2(g)?2HI(g)△H<0,并達平衡,12的轉化率a(I2)隨時間變化如圖曲線Ⅱ所示
將1.0mol I2 (g)和2.4mcl H2置于某2L密閉容器中,在某一溫度下發生反應H2(g)+I2(g)?2HI(g)△H<0,并達平衡,12的轉化率a(I2)隨時間變化如圖曲線Ⅱ所示查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 放熱反應在常溫下都很容易發生 | |
| B. | 吸熱反應不加熱就不會發生 | |
| C. | 需要加熱才能發生的反應都是吸熱反應 | |
| D. | 根據反應物和生成物具有總能量的相對大小可確定反應熱 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ①③ | C. | ①②③ | D. | ③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1L溶液中含142gNa2SO4 | B. | 1L溶液中含有1molNa+ | ||
| C. | 將142gNa2SO4溶于1L水中配成溶液 | D. | 1L水中含有1molNa2SO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 在恒溫恒容的密閉容器中,通入lmolN2和3molH2,發生反應:N2(g)+3H2(g)$?_{催化劑}^{高溫高壓}$ 2NH3(g).
在恒溫恒容的密閉容器中,通入lmolN2和3molH2,發生反應:N2(g)+3H2(g)$?_{催化劑}^{高溫高壓}$ 2NH3(g).查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com