
| A. | 100mL 1mol/LAlCl3溶液 | B. | 200 mL 1mol/LMgCl2溶液 | ||
| C. | 100mL 0.5mol/LCaCl2溶液 | D. | 100 mL 2 mol/L KCl溶液 |
分析 根據300ml 1mol/L的NaCl溶液中Cl-的物質的量濃度為1mol/L,與溶液的體積無關,以此來分析.
解答 解:由NaCl═Na++Cl-知1 mol/L NaCl溶液中,c(Cl-)=1 mol/L,
A、1 mol/LAlCl3溶液中c(Cl-)為3 mol/L,故A不符合;
B、1 mol/L MgCl2溶液中c(Cl-)為2 mol/L,故B不符合;
C、0.5 mol/L CaCl2溶液中c(Cl-)=1 mol/L,故C符合;
D、2 mol/L KCl溶液中c(Cl-)為2 mol/L,故D不符合;
故選C.
點評 本題考查物質的量濃度的計算,明確濃度與物質的構成的關系是解答本題的關鍵,并注意離子的濃度與物質的濃度有關,而與溶液的體積無關,題目難度不大.


科目:高中化學 來源: 題型:解答題
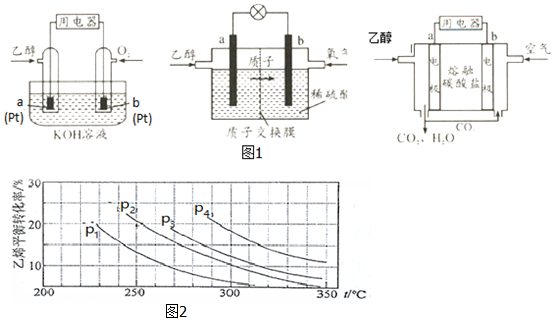
| 鍵 | C-C | C-H | O=O | H-O | C-O | C=O |
| 鍵能/(kJ•mol-1) | 348 | 413 | 498 | 463 | 351 | 799 |
| 實驗編號 | 實驗步驟 | 實驗現象 |
| 1 | 向4mL無水乙醇中加入1mL溴水,充分振蕩,靜置4小時 | 溶液橙黃色褪去,溶液接近無色 |
| 2 | 向4mL無水乙醇中加入1mL溴水,加熱至沸騰 | 開始現象不明顯,沸騰后溶液迅速褪色 |
| 向淀粉KI溶液中滴加冷卻后的上述混合液 | 溶液顏色不變 | |
| 3 | 向4mL水中加入1mL溴水,加熱至沸騰 | 橙黃色略變淺 |
| 向淀粉KI溶液中滴加冷卻后的溴水混合液 | 溶液變藍 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③④ | B. | ②③④① | C. | ③②④① | D. | ①④②③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 容器內壓強p p甲=p丙>2p乙 | |
| B. | SO3的質量m m甲=m丙<2m乙 | |
| C. | c(SO2)與c(O2)之比k k甲=k丙>2k乙 | |
| D. | 反應放出或吸收熱量的數值Q Q甲=197-Q丙>2Q乙 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯氣和水發生反應:Cl2+H2O?2H++Cl-+ClO- | |
| B. | 用NaOH溶液除去鋁表面的氧化膜時產生氣泡:2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑ | |
| C. | 金屬鈉和水反應:Na+2H2O=Na++2OH-+H2↑ | |
| D. | 將鐵粉加入稀硫酸和硝酸鉀混合溶液中,鐵粉溶解:Fe+2H+=Fe2++H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H++OH-═H2O CH3COOH+NaOH═CH3COONa+H2O | |
| B. | Ba2++SO42-═BaSO4↓ Ba(OH)2+H2SO4═BaSO4↓+2H2O | |
| C. | CO32-+2H+═CO2↑+H2O CaCO3+2HCl═CaCl2+CO2↑+H2O | |
| D. | Al(OH)3+OH-═AlO2-+2H2O Al(OH)3+NaOH═NaAlO2+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com