

| A. | 斷開1 mol O-O鍵比斷開1 mol N-N鍵所需能量少448kJ | |
| B. | 斷開1 mol H-O鍵比斷開1 mol H-N鍵所需能量相差約72.6kJ | |
| C. | 由以上鍵能的信息可知H2O的沸點比NH3高 | |
| D. | 由元素非金屬性的強弱可知 H一O鍵比H一N鍵弱 |
分析 A.氧氣中為O=O鍵,氮氣中為N≡N鍵;
B.已知4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H=-1269kJ/mol,根據焓變=反應物斷鍵吸收熱量-生成物形成化學鍵放出熱量判斷,H-O鍵與H-N的鍵能大小;
C.鍵能與沸點無關;
D.元素的非金屬性越強,與H元素形成的化學鍵越穩定.
解答 解:A.根據II可知O=O鍵的鍵能比N≡N鍵的鍵能小,則斷開1molO=O鍵比斷開1mol N≡N鍵所需能量少448kJ,故A錯誤;
B.已知4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H=-1269kJ/mol,則12H-N+3×498kJ/mol-2×946kJ/mol-12H-O=-1269kJ/mol,得(H-O)-(H-N)=72.6kJ/mol,所以斷開1mol H-O鍵與斷開1mol H-N鍵所需能量相差約72.6kJ,故B正確;
C.鍵能與沸點無關,沸點與分子間作用力有關,故C錯誤;
D.元素的非金屬性越強,與H元素形成的化學鍵越穩定,非金屬性:O>N,則H-O鍵比H-N鍵強,故D錯誤;
故選B.
點評 本題考查了化學鍵鍵能和焓變關系計算,圖象分析判斷,題目難度中等,側重于考查學生的分析能力和計算能力.


科目:高中化學 來源: 題型:解答題
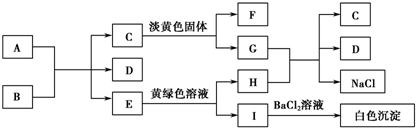
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
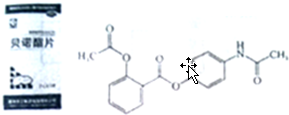
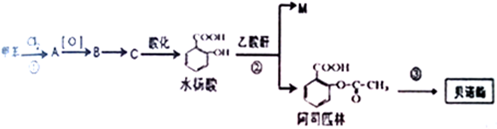
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鐵和稀硫酸反應 2Fe+6H+═2Fe3++3H2↑ | |
| B. | 向硫酸鈉溶液中滴加氯化鋇溶液 Ba2++SO42-═BaSO4↓ | |
| C. | 氯水加入到溴化鉀溶液中 Br-+Cl2═Br2+Cl- | |
| D. | 碳酸鈣溶于稀鹽酸 CO32-+2H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 日常生活中的手電筒干電池通常是鋅錳電池,其構造示意圖如下:
日常生活中的手電筒干電池通常是鋅錳電池,其構造示意圖如下:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
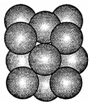 化學中的某些元素與生命活動密不可分.請回答下列問題:
化學中的某些元素與生命活動密不可分.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 人工固氮是指將氮元素由游離態轉化為化合態的過程.據報道,常溫、常壓、光照條件下,N2在摻有少量Fe2O3的TiO2催化劑表面能與水發生反應,生成的主要產物為NH3.相應的熱化學方程式為:
人工固氮是指將氮元素由游離態轉化為化合態的過程.據報道,常溫、常壓、光照條件下,N2在摻有少量Fe2O3的TiO2催化劑表面能與水發生反應,生成的主要產物為NH3.相應的熱化學方程式為:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.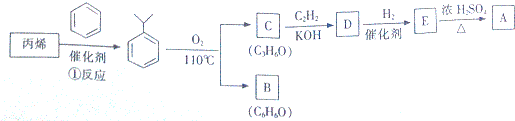
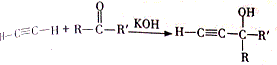
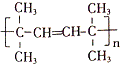 ,該反應的類型是加聚反應;B遇FeCl3溶液顯紫色,B的名稱是苯酚.
,該反應的類型是加聚反應;B遇FeCl3溶液顯紫色,B的名稱是苯酚.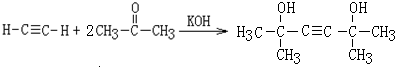 .
.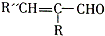 +H2O
+H2O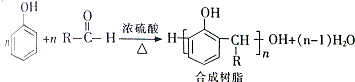
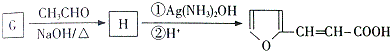
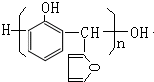 .
.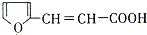 的所有同分異構體的結構簡式
的所有同分異構體的結構簡式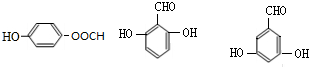 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com