
【題目】固體氧化物燃料電池是以固體氧化鋯-氧化釔為電解質,這種固體電解質在高溫下允許O2-在其間通過。該電池的工作原理如下圖所示,其中多孔電極a、b均不參與電極反應。下列判斷正確的是( )

①多孔電極a為負極
②a極對應的電極反應式為O2+2H2O+4e-==4OH-
③b極的電極反應式為H2-2e-+O2-==H2O
④該電池的總反應式為2H2+O2![]() 2H2O
2H2O
A. ①② B. ②④ C. ②③ D. ③ ④
【答案】D
【解析】①圖中電子由多孔電極b通過導線流向多孔電極a,多孔電極b為負極,多孔電極a為正極,①錯誤;②a極對應的電極反應式為O2+4e-=2O2-,②錯誤;③b極的電極反應式為H2-2e-+O2-=H2O,③正確;④根據正負極得失電子相等,將正負極電極反應式相加,該電池的總反應式為2H2+O2![]() 2H2O,④正確;正確的是③④,答案選D。
2H2O,④正確;正確的是③④,答案選D。
負極電極反應式 | 正極電極反應式 | |
酸性電解質 | H2-2e-=2H+ | O2+4e-+4H+=2H2O |
堿性電解質 | H2-2e-+2OH-=2H2O | O2+4e-+2H2O=4OH- |
熔融氧化物 | H2-2e-+O2-=H2O | O2+4e-=2O2- |
熔融碳酸鹽 | H2-2e-+CO32-=H2O+CO2 | O2+4e-+2CO2=2CO32- |


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】溫度為T時,向2.0 L恒容密閉容器中充入2.0 mol X,反應X(g) ![]() Y(g)+Z(g)經一段時間后達到平衡。反應過程中測定的部分數據見下表:
Y(g)+Z(g)經一段時間后達到平衡。反應過程中測定的部分數據見下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(Y)/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
下列說法不正確的是
A. 反應在前250 s的平均速率為v(Y)=0.000 8 mol·L-1·s-1
B. 保持其他條件不變,升高溫度,平衡時c(Y)=0.21 mol·L-1,則反應的ΔH>0
C. 相同溫度下,起始時向容器中充入4.0 mol Y、4.0 mol Z,達到平衡時,則此反應的化學平衡常數為1/20
D. 相同溫度下,若起始時向容器中充入2.0 mol X、0.40 mol Y和0.80 mol Z,則達到平衡前v(正)>v(逆)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式書寫正確的是
A. 鈉和冷水反應:Na+2H2O=Na++2OH+H2↑
B. 澄清石灰水與少量NaHCO3溶液混合:Ca2+ + OH-+ HCO3-![]() CaCO3↓+ H2O
CaCO3↓+ H2O
C. 向沸水中滴入適量的飽和氯化鐵溶液;Fe 3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
D. 碳酸氫銨溶液中加入過量氫氧化鈉溶液 HCO3-+ OH-=CO32-+ H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)0.5 mol CH4的質量為________g,約含有______個H,在標準狀況下的體積為_______L。
(2)相同質量的CO和CO2,它們所含的原子數之比為_______,在同溫同壓下,它們的密度之比為______;等物質的量的CO和CO2的混合氣體的密度是相同條件下氫氣密度的__________倍。
(3)12.4 g Na2R含Na+0.4 mol,則R的相對原子質量為_____________。
(4)已知16 g肼(N2H4)含有的電子數為b,則阿伏加德羅常數為______________。(用含b的式子表示)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向10mL0.1mol/L二元弱酸H2A溶液中滴加0.1mol/LNaOH溶液,溶液中各組分物質的量分數δ(X) [δ(X)=![]() ]隨pH的變化如圖所示。下列敘述錯誤的是
]隨pH的變化如圖所示。下列敘述錯誤的是
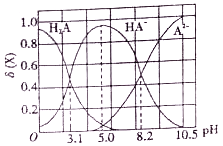
A. Ka1(H2A)為10-3.1
B. pH=5.0時,c(Na+)>c(HA-)>c(H+)>c(OH-)>c(A2-)
C. pH=8.2時,c(Na+)+c(H+)=c(OH-)+3c(A2-)
D. pH由5.0調至10.5時,主要反應的離子方程式為HA-+OH-=A2-+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】1 g碳與適量水蒸氣反應生成CO和H2,需吸收10.94 kJ熱量,此反應的熱化學方程式為( )
A. C+H2O===CO+H2 ΔH=+131.3 kJ·mol-1
B. C(s)+H2O(g)===CO(g)+H2(g) ΔH=+10.94 kJ·mol-1
C. C(s)+H2O(l)===CO(g)+H2(g) ΔH=+131.3 kJ·mol-1
D. C(s)+H2O(g)===CO(g)+H2(g) ΔH=+131.3 kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以某廢催化劑(含Al2O3 36%、CoS 20%、MoS2 20%、MgO 8%等)為原料生產Co2O3的工藝路線如下:
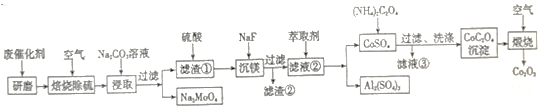
已知: 氧化鋁有兩種晶型α-Al2O3 和γ- Al2O3,α- Al2O3致密難溶于酸和堿。
(1)廢催化劑焙燒前先將其研磨,其目的是_________________________。
(2)已知“焙燒除硫”后的產物有CoO、MoO3。寫出Na2CO3溶液“浸取”過程的離子反應方程式:______________________。
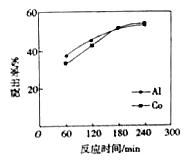
(3) 硫酸浸泡濾渣①的實驗條件為硫酸濃度12 mol/L、液固比為3、反應溫度60℃。該條件下,鋁、鈷浸出率與時間關系如圖。當浸泡時間小于180 min時,鋁、鈷浸出率隨著時間的推移均增加較快;180 min 后鋁和鈷的浸出率都提高不多,且鈷浸出率高于鋁浸出率。試解釋180min后鈷浸出率高于鋁浸出率的原因: ____________________。
(4)萃取劑對Al3+、Co2+萃取率與pH 的關系如圖。
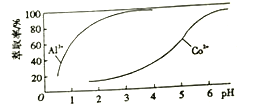
萃取分離鈷、鋁的實驗操作為: 向萃取分液后的有機相中加硫酸調pH=3~4,分液可得CoSO4溶液,___________,可得Al2(SO4)3溶液。
(5)“濾液③”主要物質的化學成分是_______ (寫化學式),用途之一為___________________。
(6)“煅燒”過程 相關反應的化學方程式為_________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】白酒、食醋、蔗糖等均為家庭廚房中常用的物質,利用這些物質能完成下列實驗的是
①驗證蛋殼能否溶于酸②檢驗白酒中是否含有甲醇③鑒別食鹽和小蘇打④檢驗自來水中是否含有氯離子
A.①②B.②④C.③④D.①③
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2 g Cu2S和CuS的混合物在酸性溶液中用400 mL 0.075 mol·L-1 KMnO4溶液處理,發生反應如下:
![]() +5Cu2S+44H+= 10Cu2++5SO2↑+8Mn2++22H2O
+5Cu2S+44H+= 10Cu2++5SO2↑+8Mn2++22H2O
![]() +5CuS+28H+ = 5Cu2++5SO2↑+6Mn2++14H2O
+5CuS+28H+ = 5Cu2++5SO2↑+6Mn2++14H2O
反應后煮沸溶液,趕盡SO2,剩余的KMnO4恰好與350 mL 0.1 mol·L-1(NH4)2Fe(SO4)2溶液完全反應。(1)配平KMnO4與(NH4)2Fe(SO4)2反應的離子方程式
______![]() +______Fe2++______H+ =______Mn2++______Fe3++______H2O
+______Fe2++______H+ =______Mn2++______Fe3++______H2O
(2)KMnO4溶液與混合物反應后,剩余KMnO4的物質的量為________mol。
(3)混合物中Cu2S的質量分數為_____________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com