
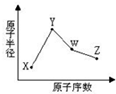
 X、Y、W、Z是四種常見的短周期元素,其原子半徑隨原子序數(shù)表化如下圖所示.已知X的一種核素的質量數(shù)為18,中子數(shù)為10,Y和Ne原子的核外電子總數(shù)相差1;W的單質是一種常見的半導體材料;Z的非金屬性在同周期主族元素中最強.
X、Y、W、Z是四種常見的短周期元素,其原子半徑隨原子序數(shù)表化如下圖所示.已知X的一種核素的質量數(shù)為18,中子數(shù)為10,Y和Ne原子的核外電子總數(shù)相差1;W的單質是一種常見的半導體材料;Z的非金屬性在同周期主族元素中最強.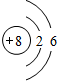 .
.分析 X、Y、W、Z是四種常見的短周期元素,已知X的一種核素的質量數(shù)為18,中子數(shù)為10,則X元素原子的質子數(shù)為18-10=8,故X為氧元素;Y和Ne原子的核外電子數(shù)相差1,X為Na或F,X原子半徑大于氧原子,故X為Na元素;W的單質是一種常見的半導體材料,原子序數(shù)大于Na元素,故W為Si元素;Z的吸引電子的能力在同周期主族元素中最大,原子序數(shù)大于Si,故Z為Cl元素.以此解答該題.
解答 解:X、Y、W、Z是四種常見的短周期元素,已知X的一種核素的質量數(shù)為18,中子數(shù)為10,則X元素原子的質子數(shù)為18-10=8,故X為氧元素;Y和Ne原子的核外電子數(shù)相差1,X為Na或F,X原子半徑大于氧原子,故X為Na元素;W的單質是一種常見的半導體材料,原子序數(shù)大于Na元素,故W為Si元素;Z的吸引電子的能力在同周期主族元素中最大,原子序數(shù)大于Si,故Z為Cl元素.
(1)W為Si,原子核外電子數(shù)為14,有3個電子層,最外層電子數(shù)為4,處于周期表中第三周期IVA族,X為O,陰離子的結構示意圖為,
故答案為:三;IVA;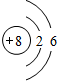 ;
;
(2)Z為Cl元素,由于元素的非金屬性Cl>Br,故氫化物穩(wěn)定性HCl>HBr,較穩(wěn)定的是HCl;由于在HF分子之間存在氫鍵,增加了分子之間的吸引力,所以物質的熔沸點較高的是HF,故答案為:HCl;HF;
(3)同周期隨原子序數(shù)增大原子半徑減小,原子失去電子的能力逐漸減弱,元素的金屬性逐漸減弱,所以金屬性Na>Mg;元素的金屬性越強,其單質與水貨酸置換出氫氣就越容易.所以可以通過Na與冷水劇烈反應,而Mg與冷水反應較慢證明元素的金屬性Na>Mg,故答案為:Na;Na與冷水劇烈反應,而Mg與冷水反應較慢;
(4)Y的最高價氧化物對應的水化物NaOH是強堿,Z的最高價氧化物對應的水化物HClO4是一元強酸,二者發(fā)生酸堿中和反應,產(chǎn)生高氯酸鈉和水,發(fā)生反應的化學反應方程式是NaOH+HClO4=NaClO4+H2O.
故答案為:NaOH+HClO4=NaClO4+H2O.
點評 本題考查原子結構與元素周期律的關系,題目難度中等,注意把握元素周期律的遞變規(guī)律以及原子核外電子的排布特點,明確元素的種類為解答該題的關鍵.


科目:高中化學 來源:2017屆江西省高三上第二次月考化學試卷(解析版) 題型:實驗題
某同學設計如下圖所示裝置來試驗用粗鐵粒與某濃度稀硝酸反應制取NO氣體。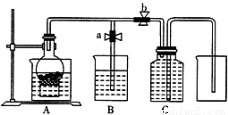
(1)當打開開關a,關閉開關b時,A中干燥管中觀察到的實驗現(xiàn)象是 ,燒杯B中盛的是 溶液。當 時關閉開關a,打開開關b,此時C中用排水法收集NO氣體。當C中收滿氣體后,關閉開關b,裝置A中觀察到的現(xiàn)象是① ;② 。
(2)將a mol Fe與含b mol HNO3的稀溶液充分反應后,若硝酸的還原 產(chǎn)物只有NO。試討論分析燒杯A中最后溶液的主要陽離子組成及其物質的量,將結果填入下表未完成的空格中。
產(chǎn)物只有NO。試討論分析燒杯A中最后溶液的主要陽離子組成及其物質的量,將結果填入下表未完成的空格中。
a/b取值范圍 | 最終溶液中的主要陽離子及其物質的量 |
<1/4 | |
=1/4 | a mol Fe3+ |
大于1/4小于3/8 | |
=3/8 | a mol Fe2+ |
>3/8 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 明礬溶于水能形成氫氧化鋁膠體,可用于自來水的殺菌消毒 | |
| B. | 鋁能置換出氧化鐵中的鐵,可用于鋼鐵工業(yè)中大量冶煉鐵 | |
| C. | 碳酸鈉具有堿性,可用于胃酸中和劑 | |
| D. | 氧化鎂熔點高,可用于耐高溫材料 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
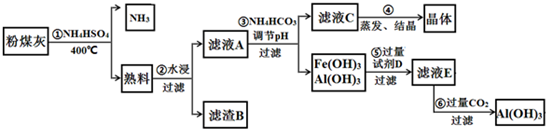
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,等體積的CH4和CO2分子數(shù)相等 | |
| B. | 與NaOH溶液、稀硫酸反應產(chǎn)生等量的H2,所需鋁粉的質量相等 | |
| C. | 常溫下,銅與濃硫酸迅速反應產(chǎn)生SO2氣體 | |
| D. | 1mol OH-和17g NH3所含的電子數(shù)相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | v(NH3)=$\frac{2}{3}$v(H2O) | B. | v(O2)=$\frac{6}{5}$v(H2O) | C. | v(NH3)=$\frac{5}{4}$v(O2) | D. | v(O2)=$\frac{4}{5}$v(NO) |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | K+ | B. | Ba2+ | C. | Zn2+ | D. | Mg2+ |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com