
| 實驗編號 | I-的初始濃度 (mol?L-1) | OCl-的初始濃度 (mol?L-1) | OH-的初始濃度 (mol?L-1) | 初始速率v (mol?L-1?s-1) |
| 1 | 2×10-3 | 1.5×10-3 | 1.00 | 1.8×10-4 |
| 2 | a | 1.5×10-3 | 1.00 | 3.6×10-4 |
| 3 | 2×10-3 | 3×10-3 | 2.00 | 1.8×10-4 |
| 4 | 4×10-3 | 3×10-3 | 1.00 | 7.2×10-4 |
| n |
| V |
| 0.0001mol |
| 0.05L |
| n |
| V |
| 0.000075mol |
| 0.05L |
| 1mol/L×0.05L |
| 0.04L |
| n |
| V |
| 1mol/L×0.05L |
| 0.04L |


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
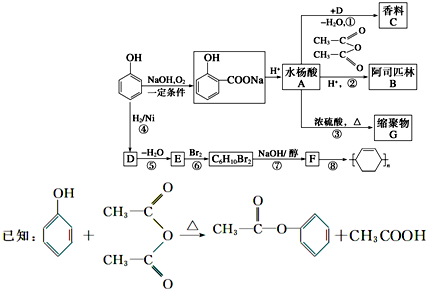
查看答案和解析>>
科目:高中化學 來源: 題型:
| 實驗編號 | 室溫下,試管中所加試劑及其用量/mL | 室溫下溶液顏色褪至無色所需時間/min | |||
| 0.6mol/L H2C2O4溶液 | H2O | 0.2mol/L KMnO4溶液 | 3mol/L 稀硫酸 | ||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
| 實驗編號 | 室溫下,試管中所加試劑及其用量/mL | 再向試管中加入少量固體 | 室溫下溶液顏色褪至無色所需時間/min | |||
| 0.6mol/L H2C2O4溶液 | H2O | 0.2mol/L KMnO4溶液 | 3mol/L 稀硫酸 | |||
| 4 | 3.0 | 2.0 | 3.0 | 2.0 | t | |
查看答案和解析>>
科目:高中化學 來源: 題型:
 次硫酸氫鈉甲醛(NaHSO2?HCHO?2H2O)在印染、醫藥以及原子能工業中應用廣泛,已知次硫酸氫鈉甲醛具有強還原性,且在120℃以上發生分解.以Na2SO3、SO2、HCHO和鋅粉為原料制備次硫酸氫鈉甲醛的實驗步驟如下:
次硫酸氫鈉甲醛(NaHSO2?HCHO?2H2O)在印染、醫藥以及原子能工業中應用廣泛,已知次硫酸氫鈉甲醛具有強還原性,且在120℃以上發生分解.以Na2SO3、SO2、HCHO和鋅粉為原料制備次硫酸氫鈉甲醛的實驗步驟如下:查看答案和解析>>
科目:高中化學 來源: 題型:
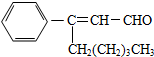 茉莉醛具有濃郁的茉莉花香,其結構簡式如圖所示,關于茉莉醛的下列敘述正確的是( )
茉莉醛具有濃郁的茉莉花香,其結構簡式如圖所示,關于茉莉醛的下列敘述正確的是( )| A、茉莉醛與苯甲醛互為同系物 |
| B、在加熱和催化劑作用下加氫,每摩爾茉莉醛最多能消耗2mol氫氣 |
| C、一定條件下,茉莉醛能被銀氨溶液、新制氫氧化銅等多種氧化劑氧化 |
| D、從理論上說,202g茉莉醛能從足量銀氨溶液中還原出216g銀 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| O2 |
| 催化劑/△ |
| H2O |
| NaOH |
| 鹽酸 |
| 鹽酸 |
| 電解 |
| O2 |
| △ |
| CO2 |
| A、②④ | B、③④ | C、①④ | D、①②③ |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com