
分析 反應中CO轉化為CO2,則n(CO)=n(CO2)=n鐵氧化物(O),產生的CO2全部用澄清石灰水吸收,得到沉淀30g為CaCO3,根據碳元素守恒n(CO2)=n(CaCO3),計算Fe的氧化物中Fe元素質量,進而計算Fe原子物質的量確定氧化物化學式.
解答 解:產生的CO2全部用澄清石灰水吸收,得到沉淀30g為CaCO3,根據碳元素守恒n(CO2)=n(CaCO3)=$\frac{30g}{100g/mol}$=0.3mol,反應中CO轉化為CO2,則n鐵氧化物(O)=n(CO)=n(CO2)=0.3mol,故Fe的氧化物中Fe元素質量=16g-0.3mol×16g/mol=11.2g,故Fe原子物質的量為$\frac{11.2g}{56g/mol}$=0.2mol,則氧化物中Fe、O原子數目之比為0.2mol:0.3mol=2:3,故該鐵的氧化物為Fe2O3,
答:該鐵的氧化物為Fe2O3.
點評 本題考查化學方程式有關計算,明確反應過程是解題關鍵,注意利用守恒法進行解答,難度中等.


科目:高中化學 來源: 題型:解答題
| 配料表 | 精制海鹽、碘酸鉀[ |
| 含碘量 | 20~40mg/kg |
| 衛生許可證號 | ××衛碘字(1999)第001號 |
| 分裝日期 | 見封底 |
| 儲藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹調時,待食品熟后加入碘鹽 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | X分子中最多可有9個碳原子共平面 | |
| B. | X可以發生取代、加成、聚合等反應 | |
| C. | 1 mol X與足量NaHCO3溶液反應所得物質的分子式為C9H7O4Na | |
| D. | 苯環上的取代基與X完全相同的X的同分異構體有4種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 某離子第三層上和第二層上的電子數均為第一層的4倍 | |
| B. | Cl-的結構示意圖: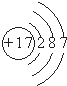 | |
| C. | 某物質的焰色反應為黃色,某物質一定為鈉的化合物 | |
| D. | 14C和14N的質量數相等,互稱為同位素 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe的質量為2.7g,Al的質量為2.8g | B. | Fe的質量為2.8g,Al的質量為2.7g | ||
| C. | Fe的質量為5.4g,Al的質量為5.6g | D. | Fe的質量為5.6g,Al的質量為5.4g |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
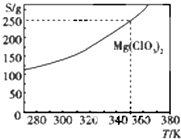 Mg(ClO3)2在農業上可用做脫葉劑、催熟劑.可采用復分解反應制備:MgCl2+2NaClO3═Mg(ClO3)2+2NaCl.已知Mg(ClO3)2的溶解度(S)隨溫度(T)的變化曲線如圖所示.下列有關敘述中不正確的是( )
Mg(ClO3)2在農業上可用做脫葉劑、催熟劑.可采用復分解反應制備:MgCl2+2NaClO3═Mg(ClO3)2+2NaCl.已知Mg(ClO3)2的溶解度(S)隨溫度(T)的變化曲線如圖所示.下列有關敘述中不正確的是( )| A. | 溫度越高,Mg(ClO3)2飽和溶液的物質的量濃度越大 | |
| B. | 溫度越高,Mg(ClO3)2飽和溶液的質量分數越大 | |
| C. | 350K時,Mg(ClO3)2飽和溶液的物質的量濃度為$\frac{250g}{191g/mol×1L}$ | |
| D. | 350 K時,Mg(ClO3)2飽和溶液的質量分數為$\frac{250g}{350g}$×100% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Sn2+、Fe2+、Ge3+ | B. | Sn2+、Ge3+、Fe2+ | C. | Ge3+、Fe2+、Sn2+ | D. | Fe2+、Sn2+、Ge3+ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com