
 紅磷P(s)和Cl2(g)發生反應生成PCl3(g),繼續反應生成PCl5(g).反應過程和能量關系如圖所示(圖中的△H表示生成1mol產物的數據).
紅磷P(s)和Cl2(g)發生反應生成PCl3(g),繼續反應生成PCl5(g).反應過程和能量關系如圖所示(圖中的△H表示生成1mol產物的數據).分析 (1)由圖象可知,1molPCl3分解為1molP與1molCl2反應吸收306kJ的能量;
(2)分解為PCl5為0.8mol-0.60mol=0.2mol,進而計算PCl5的分解率;由圖可知,PCl5的分解反應為吸熱反應,升高溫度平衡正向移動,PCl5的分解率增大;
(3)兩步反應均為放熱反應,降溫有利于提高產率,防止產物分解;
(4)PCl5與足量水充分反應,最終生成兩種酸,生成磷酸與HCl.
解答 解:(1)由圖象可知,1molPCl3分解為1molP與1molCl2反應吸收306kJ的能量,則PCl3分解成P和Cl2的熱化學方程式是:PCl3(g)═P (s)+$\frac{3}{2}$Cl2(g)△H=+306 kJ/mol,
故答案為:PCl3(g)═P (s)+$\frac{3}{2}$Cl2(g)△H=+306 kJ/mol;
(2)分解為PCl5為0.8mol-0.60mol=0.2mol,PCl5的分解率α1=$\frac{0.2mol}{0.8mol}$×100%=25%;
由圖可知,PCl5的分解反應為吸熱反應,升高溫度平衡正向移動,PCl5的分解率增大,故α2>α1,
故答案為:25%;大于;
(3)先將P和Cl2反應生成中間產物PCl3,然后降溫,再和Cl2反應生成PCl5,是因為:兩步反應均為放熱反應,降溫有利于提高產率,防止產物分解,
故答案為:兩步反應均為放熱反應,降溫有利于提高產率,防止產物分解;
(4)PCl5與足量水充分反應,最終生成兩種酸,生成磷酸與HCl,反應方程式為:PCl5+4H2O═H3PO4+5HCl,
故答案為:PCl5+4H2O═H3PO4+5HCl.
點評 本題考查化學平衡計算與影響因素、熱化學方程式等,需要學生具備扎實的基礎與靈活應用能力.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 原鐵和鋁的物質的量相等 | |
| B. | 原鹽酸的濃度為2mol•L-1 | |
| C. | 鐵加入鹽酸中的離子方程式為2Fe+6H+=2Fe3++3H2↑ | |
| D. | 鹽酸與氫氧化鈉溶液的物質的量濃度之比為1:3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 達到化學平衡時,N2將完全轉化為NH3 | |
| B. | 達到化學平衡時,N2、H2和NH3的物質的量濃度一定相等 | |
| C. | 達到化學平衡時,正反應和逆反應的速率都為零 | |
| D. | 達到化學平衡時,N2和H2的轉化率相同且c(N2):c(H2)=1:3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 在80℃時,將0.4mol的四氧化二氮氣體充入2L已抽空的固定容積的密閉容器中,隔一段時間對該容器內的物質進行分析,得到如下數據:
在80℃時,將0.4mol的四氧化二氮氣體充入2L已抽空的固定容積的密閉容器中,隔一段時間對該容器內的物質進行分析,得到如下數據:時間(s) C(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
| C(N2O4) | 0.20 | a | 0.10 | c | d | e |
| C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 短周期元素X.Y.Z.W在元素周期表中的相對位置如圖所示,其中w原子的最外層電子數是最內層電子數的3倍.下列判斷不正確的是( )
短周期元素X.Y.Z.W在元素周期表中的相對位置如圖所示,其中w原子的最外層電子數是最內層電子數的3倍.下列判斷不正確的是( )| A. | x與同主族且相鄰元素的氣態氫化物的沸點,前者高于后者 | |
| B. | 含Y元素的鹽溶液有的顯酸性,有的顯堿性 | |
| C. | x的氣態氫化物與w的最高價氧化物的水化物反應只能生成一種鹽 | |
| D. | x與H、O元素形成的化合物可以組成一種鹽,其中X.H.O元素原子個數之比為2:4:3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將40gNaOH溶解于1L水中配成的NaOH溶液 | |
| B. | 常溫常壓下將22.4LHCl氣體溶于水配成1L的鹽酸溶液 | |
| C. | 將1 L0.5mol/L的濃鹽酸加熱濃縮為0.5L | |
| D. | 從1000mL 1mol/L NaCl溶液中取出100 mL的溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 元素 | o | p | |
| 電離能kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1 509 | 1 561 | |
| I3 | 3 248 | 2 957 | |
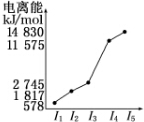
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 都能溶于濃鹽酸或濃硝酸中 | |
| B. | 都能溶于氫氧化鈉溶液中 | |
| C. | 它們的熔點都很高,常用做耐火材料 | |
| D. | 常溫下都不能與水反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com