
| A. | 標準狀況下,11.2L的戊烷所含的分子數為0.5NA | |
| B. | 28g乙烯所含共用電子對數目為5NA | |
| C. | 1 mol甲基的電子數目為7NA | |
| D. | 現有乙烯、丙烯、丁烯的混合氣體共14g,其所含原子總數為3NA |
分析 A、標況下戊烷為液體;
B、求出乙烯的物質的量,然后根據1mol乙烯中含6mol共用電子對來分析;
C、甲基不顯電性;
D、乙烯、丙烯和丁烯的最簡式均為CH2.
解答 解:A、標況下戊烷為液體,故不能根據氣體摩爾體積來計算其物質的量和分子數,故A錯誤;
B、28g乙烯的物質的量為1mol,而1mol乙烯中含6mol共用電子對,即含6NA對,故B錯誤;
C、甲基不顯電性,故1mol甲基中含9NA個電子,故C錯誤;
D、乙烯、丙烯和丁烯的最簡式均為CH2,故14g混合物中含有的CH2的物質的量為n=$\frac{14g}{14g/mol}$=1mol,故含3NA個原子,故D正確.
故選D.
點評 本題考查了阿伏伽德羅常數的有關計算,掌握物質的量的計算公式和物質結構是解題關鍵,難度不大.


 七星圖書口算速算天天練系列答案
七星圖書口算速算天天練系列答案 初中學業考試導與練系列答案
初中學業考試導與練系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 元素 | 結構或性質信息 |
| X | 其原子最外層電子數是內層電子數的2倍 |
| Y | 基態原子最外層電子排布為nsnnpn+1 |
| Z | 非金屬元素,其單質為固體,在氧氣中燃燒時有明亮的藍紫色火焰 |
| M | 單質在常溫、常壓下是氣體.基態原子的M層上有1個未成對的p電子 |
| Q | 其與X形成的合金為目前用量最多的金屬材料 |
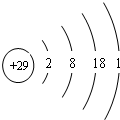 .
.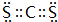 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

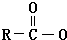 Na+NaOH$→_{△}^{CaO}$R-H+Na2CO3
Na+NaOH$→_{△}^{CaO}$R-H+Na2CO3 ,K的結構簡式為
,K的結構簡式為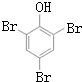 .
.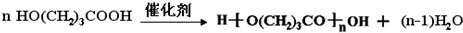 ;
;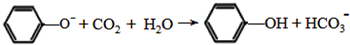 .
. (寫結構簡式).
(寫結構簡式).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 隨著元素原子序數的遞增,原子最外層電子總是從1到8重復出現 | |
| B. | 隨著元素原子序數的遞增,同周期從左到右原子半徑從小到大(稀有氣體除外)發生周期性變化 | |
| C. | 隨著元素原子序數的遞增,元素最高正價從+1到+7、負價從-7到-1重復出現 | |
| D. | 元素原子核外電子排布的周期性變化是導致原子半徑、元素主要化合價和元素性質周期性變化的主要原因 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | O2分子間存在著非極性共價鍵 | |
| B. | CO2分子內存在著極性共價鍵 | |
| C. | SO2與H2O反應的產物是離子化合物 | |
| D. | 鹽酸中含有H+和Cl-,故HCl為離子化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 從左向右數第七縱行是ⅦA族 | |
| B. | 從左向右數第十一縱行是ⅠB族 | |
| C. | ⅠA族全部是金屬元素 | |
| D. | 第ⅦA族元素從上到下,其氫化物的穩定性逐漸增強 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 工業上電解飽和食鹽水的陽極反應為:2Cl--2e-═Cl2↑ | |
| B. | 船底鑲嵌鋅塊,鋅作負極,以防船體被腐蝕 | |
| C. | 鋼鐵吸氧腐蝕的正極反應為:O2+2H2O+4e-═4OH- | |
| D. | 鐵表面鍍鋅,鐵作陽極 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 正極為Fe、負極為Fe,電解質溶液為FeCl3溶液 | |
| B. | 正極為Ag、負極為Fe,電解質溶液為CuSO4溶液 | |
| C. | 正極為Fe、負極為Zn,電解質溶液為Fe2(SO4)3溶液 | |
| D. | 正極為C、負極為Fe,電解質溶液為Fe(NO3)3溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com