

 .
.

 撲熱息痛的結構簡式為
撲熱息痛的結構簡式為


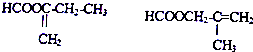
分析 B和HCN反應生成CH3C(OH)CNCH3,則B的結構簡式為CH3COCH3,A發生氧化反應生成丙酮和苯酚,則A的結構簡式為 ,D物質其質譜圖顯示相對分子質量為100,10gD的物質的量=$\frac{10g}{100g/mol}$=0.1mol,生成二氧化碳的物質的量=$\frac{22.0g}{44g/mol}$=0.5mol,生成水的物質的量=$\frac{7.2g}{18g/mol}$=0.4mol,
,D物質其質譜圖顯示相對分子質量為100,10gD的物質的量=$\frac{10g}{100g/mol}$=0.1mol,生成二氧化碳的物質的量=$\frac{22.0g}{44g/mol}$=0.5mol,生成水的物質的量=$\frac{7.2g}{18g/mol}$=0.4mol,
則D分子中含有5個C原子、8個H原子,D的相對分子質量為100,則D中還含有O原子,O原子個數=$\frac{100-12×5-1×8}{16}$=2,所以D的分子式為C5H8O2,其不飽和度=$\frac{5×2+2-8}{2}$=3,D能發生加聚反應說明含有碳碳雙鍵或三鍵,酸性條件下CH3C(OH)CNCH3和甲醇發生酯化反應,同時自身發生消去反應,則D的結構簡式為CH2=C(CH3)COOCH3,D發生加聚反應生成E,則E的結構簡式為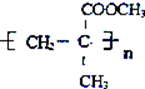 ,
,
根據題給信息知,CH2=C(CH3)COOH和SOCl反應生成G,G的結構簡式為CH2=C(CH3)COCl,H發生加聚反應生成含撲熱息痛高分子藥物,則H的結構簡式為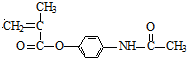 ,G和撲熱息痛反應生成H,則撲熱息痛結構簡式為
,G和撲熱息痛反應生成H,則撲熱息痛結構簡式為 ,再結合題目分析解答.
,再結合題目分析解答.
解答 解:B和HCN反應生成CH3C(OH)CNCH3,則B的結構簡式為CH3COCH3,A發生氧化反應生成丙酮和苯酚,則A的結構簡式為 ,D物質其質譜圖顯示相對分子質量為100,10gD的物質的量=$\frac{10g}{100g/mol}$=0.1mol,生成二氧化碳的物質的量=$\frac{22.0g}{44g/mol}$=0.5mol,生成水的物質的量=$\frac{7.2g}{18g/mol}$=0.4mol,
,D物質其質譜圖顯示相對分子質量為100,10gD的物質的量=$\frac{10g}{100g/mol}$=0.1mol,生成二氧化碳的物質的量=$\frac{22.0g}{44g/mol}$=0.5mol,生成水的物質的量=$\frac{7.2g}{18g/mol}$=0.4mol,
則D分子中含有5個C原子、8個H原子,D的相對分子質量為100,則D中還含有O原子,O原子個數=$\frac{100-12×5-1×8}{16}$=2,所以D的分子式為C5H8O2,其不飽和度=$\frac{5×2+2-8}{2}$=3,D能發生加聚反應說明含有碳碳雙鍵或三鍵,酸性條件下CH3C(OH)CNCH3和甲醇發生酯化反應,同時自身發生消去反應,則D的結構簡式為CH2=C(CH3)COOCH3,D發生加聚反應生成E,則E的結構簡式為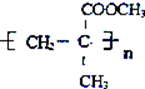 ,
,
根據題給信息知,CH2=C(CH3)COOH和SOCl反應生成G,G的結構簡式為CH2=C(CH3)COCl,H發生加聚反應生成含撲熱息痛高分子藥物,則H的結構簡式為 ,G和撲熱息痛反應生成H,則撲熱息痛結構簡式為
,G和撲熱息痛反應生成H,則撲熱息痛結構簡式為 ,
,
(1)通過以上分析知,A的結構簡式為 ,撲熱息痛結構簡式為
,撲熱息痛結構簡式為 ,
,
故答案為: ;
; ;
;
(2)通過以上分析知,該反應為加成反應,故答案為:加成;
(3)C6H6O為苯酚,能殺菌消毒,故答案為:殺菌消毒;
(4)通過以上分析知,D的結構簡式為CH2=C(CH3)COOCH3,D中官能團為碳碳雙鍵和酯基,D發生加成反應生成E,反應方程式為 ,
,
故答案為:碳碳雙鍵和酯基; ;
;
(5)含撲熱息痛高分子藥物與足量氫氧化鈉溶液發生取代反應,反應方程式為 ,
,
故答案為: ;
;
(6)D的結構簡式為CH2=C(CH3)COOCH3,D的同分異構體符合下列條件,①與D具有相同官能團說明含有酯基和碳碳雙鍵,②能發生眼鏡反應,說明含有甲酯基,③H核磁共振譜中有四種不同環境的氫原子比例分別為1:2:2:3,說明該分子中含有4種類型的H原子,符合條件的D的同分異構體有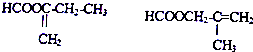 ,故答案為:
,故答案為: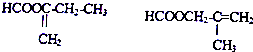 .
.
點評 本題考查有機物推斷,側重考查學生分析能力、推斷能力,以CH3C(OH)CNCH3為突破口采用正逆結合的方法推導,知道常見有機物的官能團及能夠發生的反應,注意結合題給信息分析解答,難點是同分異構體種類的判斷,題目難度中等.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | 36g鎂在足量的氮氣中完全燃燒共轉移的電子數為3NA | |
| B. | 室溫下,21.0g乙烯和丁烯的混合氣體中含有的C-H共價鍵數目為3NA | |
| C. | 標準狀況下,44.8 L NO與22.4 LO2混合后氣體中分子總數為3NA | |
| D. | 1 molNa2O和Na2O2混合物中含有的陰、陽離子總數是3NA |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 一定不存在Ba2+,NH4+可能存在 | B. | CO32-一定存在 | ||
| C. | Na+一定存在 | D. | 一定不存在Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化合反應 | B. | 置換反應 | C. | 氧化還原反應 | D. | 復分解反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
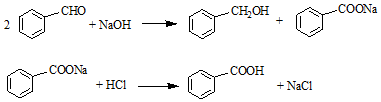
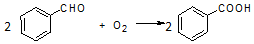
| 名稱 | 分子量 | 性狀 | 相對密度 (g•cm-3) | 沸點 (℃) | 溶解度 | ||
| 水 | 乙醚 | ||||||
| 苯甲醛 | 106 | 無色液體 | 1.04 | 179 | 微溶 | 易溶 | |
| 苯甲酸 | 122 | 無色晶體 | 1.27 | 249 | 0.21g | 66g | |
| 苯甲醇 | 108 | 無色液體 | 1.04 | 205 | 微溶 | 易溶 | |
| 乙醚 | 74 | 無色液體. | 0.71 | 35 | 不溶 | -- | |
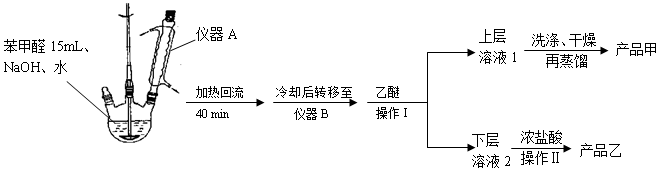
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

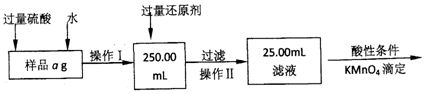
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
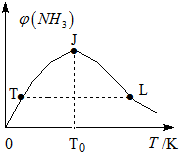 氫氣是新型能源和重要化工原料.
氫氣是新型能源和重要化工原料.| 容器編號 | 起始時各物質的物質的量/mol | 平衡時反應中的能量變化 | ||
| H2 | N2 | NH3 | ||
| Ⅰ | 3n | n | 0 | 放出熱量a kJ |
| Ⅱ | 3n | 2n | 0 | 放出熱量b kJ |
| Ⅲ | 6n | 2n | 0 | 放出熱量c kJ |
| 時間/min | 0 | 5 | 10 | 15 | 20 | 25 | … |
| NH3/mol | 2 | 1.0 | 0.5 | 0.25 | 0.24 | 0.24 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
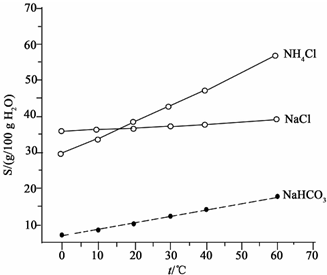
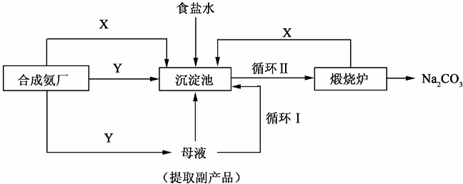
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | x=0.6a 2Fe2++Cl2=2Fe3++2Cl- | |
| B. | x=a 2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- | |
| C. | x=0.4a 2Br-+Cl2=Br2+2Cl- | |
| D. | x=2a 2Fe2++6Br-+4Cl2=3Br2+2Fe3++8Cl- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com