
分析 (1)3FeS2+8O2=6SO2+Fe3O4中,只有O元素的化合價降低,利用化合價計算轉移電子;
(2)KClO與Fe3+反應生成K2FeO4和KCl,結合電荷守恒和原子守恒書寫;
(3)氯化鐵具有氧化性,碘化氫具有還原性,二者發生氧化還原反應生成氯化亞鐵和碘單質;
(4)高溫條件下,氫氧化鉀與二氧化錳、氧氣反應生成錳酸鉀和水;
(5)鐵先與Fe3+反應,然后再與氫離子反應,結合反應的離子方程式計算.
解答 解:(1)3FeS2+8O2=6SO2+Fe3O4中,有3mol FeS2參加反應,8mol氧氣參加反應,只有O元素的化合價降低,則轉移電子為8mol×2×[0-(-2)]=32mol,
故答案為:32;
(2)在KOH溶液中,KClO與Fe3+反應生成K2FeO4和KCl,反應的離子方程式為:3ClO-+2Fe3++10OH-=2FeO42-+3Cl-+5H2O;
故答案為:3ClO-+2Fe3++10OH-=2FeO42-+3Cl-+5H2O;
(3)氯化鐵具有氧化性,碘化氫具有還原性,二者發生氧化還原反應生成氯化亞鐵和碘單質,反應離子方程式為:2Fe3++2I-=2Fe2++I2,
故答案為:2Fe3++2I-=2Fe2++I2;
(4)高溫條件下,氫氧化鉀與二氧化錳、氧氣反應生成錳酸鉀和水,其反應的方程式為:4KOH+2MnO2+O2=2K2MnO4+2H2O;
故答案為:4KOH+2MnO2+O2=2K2MnO4+2H2O;
(5)氫氣的物質的量為 0.1mol,
由關系式Fe~~~~2HCl~~~H2,得到
0.1mol 0.2mol 0.1mol
根據氯原子守恒,所以氯化鐵的物質的量為$\frac{1}{3}$×(0.16L×5mol/L-0.2mol)=0.2mol,
Fe~~~2FeCl3
0.1mol 0.2mol
所以參加反應的鐵粉的質量為(0.1mol+0.1mol)×56g/mol=11.2g,
故答案為:11.2g.
點評 本題綜合考查氧化還原反應、化學方程式和離子方程式的書寫、元素化合物知識等,側重學生的分析、計算能力的考查,注意把握物質的性質,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 常溫下pH=7的溶液中:Fe3+,Mg2+,SO42-,Cl-能大量共存 | |
| B. | 常溫下水電離出c(H+)×c(OH-)=10-10的溶液中:Na+,NH4+,CH3COO-,F-不能大量共存 | |
| C. | 在含有HCO3-,HSO3-,CH3COO-,S2-四種陰離子的溶液中加入足夠的Na2O2固體后,S2-濃度變化最小 | |
| D. | SO2,O2,HCl,CO2四種氣體,可以大量共存于同一容器中 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
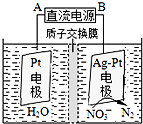 為治理環境,減少霧霾,工業上通常用下列方法治理CO2和硫、氮氧化物的污染.
為治理環境,減少霧霾,工業上通常用下列方法治理CO2和硫、氮氧化物的污染.查看答案和解析>>
科目:高中化學 來源: 題型:解答題



 +H2O$→_{△}^{稀H_{2}SO_{4}}$
+H2O$→_{△}^{稀H_{2}SO_{4}}$ +CH3OH③F→G:2
+CH3OH③F→G:2 +O2 $→_{△}^{Cu}$2
+O2 $→_{△}^{Cu}$2 +2H2O
+2H2O 等
等查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 括號內為雜質 | 除雜試劑 | 除雜操作 |
| A | Na2O2(Na2O)固體 | O2 | 在純氧氣中加熱 |
| B | Na2CO3(NaHCO3) 溶液 | CO2 | 通入過量的CO2 |
| C | FeCl3(FeCl2)溶液 | Cl2 | 通入過量的Cl2 |
| D | FeSO4(CuSO4)溶液 | Fe | 加入過量的Fe粉,充分反應后過濾 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 若a=b+c時,B的物質的量分數不變 | B. | 若a<b+c時,A的轉化率減小 | ||
| C. | 若a<b+c時,B的物質的量濃度減小 | D. | 若a>b+c時,A的物質的量分數減小 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com