
分析 (1)白色沉淀為CaCO3,根據碳元素守恒計算n(CO2),混合氣體通入盛有足量過氧化鈉的干燥管,發生反應:2Na2O2+2CO2=O2+2Na2CO3,固體增重相當于與CO2等物質的量的CO的質量,發生反應:2Na2O2+2H2O=4NaOH+O2,固體增重相當于與H2O等物質的量的氫氣的質量,根據干燥管質量增重,計算水的物質的量,再根據C、H原子守恒計算烴分子中C、H原子數目,進而確定烴的分子式;
(2)若分子中N(H)=2N(C)+2,則為烷烴.
解答 解:(1)白色沉淀為CaCO3,根據碳元素守恒n(CO2)=n(CaCO3)=$\frac{100g}{100g/mol}$=1mol;
混合氣體通入盛有足量過氧化鈉的干燥管,發生反應:2Na2O2+2CO2=O2+2Na2CO3,固體增重相當于與CO2等物質的量的CO的質量,即增重為1mol×28g/mol=28g,故過氧化鈉與水反應時增重為30g-28g=2g,發生反應:2Na2O2+2H2O=4NaOH+O2,固體增重相當于與H2O等物質的量的氫氣的質量,故n(H2O)=n(H2)=$\frac{2g}{2g/mol}$=1mol,
根據原子守恒可知,烴分子中N(C)=$\frac{1mol}{0.5mol}$=2、N(H)=$\frac{1mol×2}{0.5mol}$=4,故該烴的化學式為C2H4,
故答案為:C2H4;
(2)若為烷烴,2個碳原子需要6個H原子飽和,故不屬于烷烴,故答案為:否;若為烷烴,2個碳原子需要6個H原子飽和.
點評 本題考查有機物分子式確定的計算,注意利用差量法理解二氧化碳、水與過氧化鈉反應固體增重問題,側重考查學生分析計算能力,難度中等.


 應用題天天練四川大學出版社系列答案
應用題天天練四川大學出版社系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 升高溫度 | B. | 增大壓強 | C. | 增大NH3的濃度 | D. | 使用催化劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在現實生活中,電化學腐蝕要比化學腐蝕嚴重的多,危害更大 | |
| B. | 在銅的精煉裝置中,通常用粗銅作作陽極,精銅作陰極 | |
| C. | 氯堿工業,主要依托電解熔融的氯化鈉來制取工業上重要的化工原料燒堿和氯氣 | |
| D. | 可充電的電池稱“二次電池”,在充電時,是將電能轉變成化學能,在放電時,又將化學能轉化成電能 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1mol•L-1醋酸,溶液的pH=1 | |
| B. | 0.1mol•L-1醋酸加水稀釋,溶液中離子濃度都減小 | |
| C. | 0.1mol•L-1氨水溶液中:c(OH-)=c(NH${\;}_{4}^{+}$) | |
| D. | 0.1mol•L-1氨水與0.1mol•L-1 HCl溶液等體積混合所得溶液中:c(Cl-)>c(NH${\;}_{4}^{+}$)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
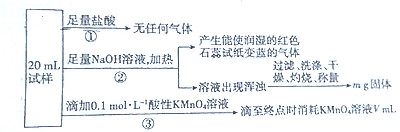
| A. | 由實驗①可推斷原混合溶液中一定不存在${NO}_{2}^{-}$、${CO}_{3}^{2-}$ | |
| B. | 由實驗①③可推斷原混合溶液中一定存在Fe2+,一定不存在${NO}_{3}^{-}$ | |
| C. | 原混合溶液中肯定存在${NH}_{4}^{+}$、Fe2+、${SO}_{4}^{2-}$ | |
| D. | 如果給出m、V的具體數據,可以確定Al3+、Fe3+是否存在 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 與HCN反應引入:
與HCN反應引入: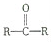 $→_{一定條件}^{HCN}$
$→_{一定條件}^{HCN}$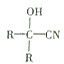
 $→_{一定條件①}^{HCN}$ A $→_{②}^{H_{2}O,H+}$ B$→_{③}^{濃H_{2}SO_{4},△}$ C $→_{催化劑④}^{聚合}$ D
$→_{一定條件①}^{HCN}$ A $→_{②}^{H_{2}O,H+}$ B$→_{③}^{濃H_{2}SO_{4},△}$ C $→_{催化劑④}^{聚合}$ D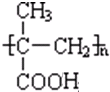 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 晶體硅是制造太陽能電池的常用材料 | |
| B. | 二氧化硅是制造光導纖維的材料 | |
| C. | 氫氟酸可用刻蝕玻璃 | |
| D. | 硅是制取水泥的原料 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com