
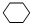
 ,名稱是環己烷.
,名稱是環己烷.分析 根據C元素、H元素守恒確定該烴的分子式為C6H12,不飽和度為1,若該烴不能使溴水或高錳酸鉀溶液褪色,說明烴中不含不飽和鍵,該烴為環烷烴,但在一定條件下,可以和液溴發生取代反應,其一溴取代物只有一種,說明分子中只有一種H原子,該烴為環己烷;
若該烴能使溴水褪色,說明分子中含有1個C=C雙鍵,該烴屬于烯烴,在催化劑作用下與H2發生加成反應,生成2,2-二甲基丁烷,則該烴的結構簡式為(CH3)3C-CH=CH2.
解答 解:n(烴):n(C):n(H)=n(烴):n(CO2):2n(H2O)=0.1mol:0.6mol:0.6mol×2=1:6:12,即1個分子中含有6個C原子、12個H原子,故該烴的分子式為C6H12;
該烴的不飽和度為1,若該烴不能使溴水或高錳酸鉀溶液褪色,說明烴中不含不飽和鍵,故該烴為環烷烴,其一溴取代物只有一種,說明分子中只有一種H原子,該烴為環己烷,結構簡式為 ;
;
若該烴能使溴水褪色,說明分子中含有1個C=C雙鍵,該烴屬于烯烴,在催化劑作用下與H2發生加成反應,生成2,2-二甲基丁烷,則該烴的結構簡式為(CH3)3C-CH=CH2,名稱為:3,3-二甲基-1-丁烯,
故答案為:C6H12;環烷烴; ;環己烷;烯烴;(CH3)3C-CH=CH2; 3,3-二甲基-1-丁烯.
;環己烷;烯烴;(CH3)3C-CH=CH2; 3,3-二甲基-1-丁烯.
點評 本題考查有機物的推斷,側重于分子式的確定、烯烴的性質與命名等,比較基礎,注意掌握燃燒法根據原子守恒確定有機物分子式,注意對基礎知識的理解掌握.


 百年學典課時學練測系列答案
百年學典課時學練測系列答案科目:高中化學 來源: 題型:選擇題
| A. | 將少量SO2氣體通入NaClO溶液中:SO2+H2O+2ClO-=SO32-+2HClO | |
| B. | 將2molSO3氣體通入一密閉容器中,達平衡后吸收QkJ熱量,則該反應的熱化學方程式為:2SO3(g)?2SO2(g)+O2(g)△H=+Q kJ/mol | |
| C. | 向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反應:4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2 | |
| D. | 用惰性電極電解MgCI2溶液:2 Cl-+2H2O=CI2↑+H2↑+2OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋁溶于氫氧化鈉溶液:Al+2OH-+H2O═AlO2-+2H2↑ | |
| B. | 銅片投入少量FeCl3溶液中:3Cu+2Fe3+═2Fe+3Cu2+ | |
| C. | Ca(HCO3)2溶液與足量澄清石灰水混合:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| D. | 用鐵棒作電極電解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;電解\;}}{\;}$2Cu↓+O2↑+4H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 A(g)+3B(g)?2C(g)反應在密閉容器中進行,若保持容積不變,在溫度分別為T1和T2時,達到平衡,B的體積分數與時間的關系如圖所示,現象一體積可變的密閉容器中通入等物質的量的A氣體和B氣體,在恒溫條件下發生反應發到平衡狀態Ⅰ后,再升高溫度,繼續反應一段時間后達到平衡狀態Ⅱ.下列敘述中正確的是( )
A(g)+3B(g)?2C(g)反應在密閉容器中進行,若保持容積不變,在溫度分別為T1和T2時,達到平衡,B的體積分數與時間的關系如圖所示,現象一體積可變的密閉容器中通入等物質的量的A氣體和B氣體,在恒溫條件下發生反應發到平衡狀態Ⅰ后,再升高溫度,繼續反應一段時間后達到平衡狀態Ⅱ.下列敘述中正確的是( )| A. | T1>T2,該反應生成物的總能量高于反應物的總能量 | |
| B. | 該反應在高溫時才能自發進行 | |
| C. | 由平衡狀態Ⅰ到平衡狀態Ⅱ的過程中,平衡向逆向移動,A的體積分數一直沒有變化 | |
| D. | 反映從開始到平衡狀態Ⅱ的過程中,平衡常數K和A的轉化率都是先增大后減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 溫度 | 25 | t1 | t2 |
| 水的離子積 | 1×10-14 | a | 1×10-12 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,16g14CH4所含中子數目為8NA | |
| B. | 標準狀況下,7.8g苯中含碳碳雙鍵的數目為0.3 NA | |
| C. | 含0.2NA個陰離子的Na2O2和水完全反應轉移0.2mol電子 | |
| D. | 0.1L 3mol•L-1的NH4NO3溶液中含有的NH4+數目為0.3N |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 高壓的條件下,有利于工業上氨氣的合成 | |
| B. | 高壓比常壓有利于合成SO3的反應 | |
| C. | 由H2、I2(g)、HI(g)氣體組成的平衡體系加壓后顏色變深 | |
| D. | 黃綠色的氯水光照后顏色變淺 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com