
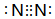 .
. NH3•H2O
NH3•H2O  NH4++OH-.
NH4++OH-.分析 W、X、Y、Z是原子序數依次增大的四種短周期元素.W的氣態氫化物能使紫色石蕊溶液變藍,則W為N元素,W和X兩種元素的最高價氧化物的水化物均能與Y的氫氧化物發生反應,應是氫氧化鋁與強酸、強堿之間的反應,可以推斷X為Na、Y為Al.由于W、X、Y、Z的最外層電子數之和為16,可知Z原子最外層電子數為16-5-1-3=7,由原子序數知Z處于第三周期,故Z為Cl,據此解答.
解答 解:W、X、Y、Z是原子序數依次增大的四種短周期元素.W的氣態氫化物能使紫色石蕊溶液變藍,則W為N元素,W和X兩種元素的最高價氧化物的水化物均能與Y的氫氧化物發生反應,應是氫氧化鋁與強酸、強堿之間的反應,可以推斷X為Na、Y為Al.由于W、X、Y、Z的最外層電子數之和為16,可知Z原子最外層電子數為16-5-1-3=7,由原子序數知Z處于第三周期,故Z為Cl.
(1)W單質為N2,其電子式是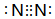 ,故答案為:
,故答案為: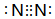 ;
;
(2)W的氣態氫化物能使紫色石蕊溶液變藍的原因:NH3+H2O  NH3•H2O
NH3•H2O  NH4++OH-,
NH4++OH-,
故答案為:NH3+H2O  NH3•H2O
NH3•H2O  NH4++OH-;
NH4++OH-;
(3)As元素的原子序數為33,與W在同一主族,As在元素周期表中的位置是:第四周期 第VA族,
故答案為:第四周期 第VA族;
(4)W的最高價氧化物的水化物為HNO3,Y的氫氧化物為Al(OH)3,二者發生反應的離子方程式是:3H++Al(OH)3═Al3++3H2O,
故答案為:3H++Al(OH)3═Al3++3H2O;
(5)X與Z的單質之間發生的反應是鈉在氯氣中燃燒生成氯化鈉,反應的化學方程式是:2Na+Cl2$\frac{\underline{\;點燃\;}}{\;}$2NaCl,
故答案為:2Na+Cl2$\frac{\underline{\;點燃\;}}{\;}$2NaCl;
(6)已知Q與Z(Cl))是位于相鄰周期的同主族元素,則Q為Br,由KQ<KZ可知Q的氣態氫化物的穩定性弱于Z,故Q的非金屬性弱于Z,
故答案為:Br;由KQ<KZ可知Q的氣態氫化物的穩定性弱于Z,故Q的非金屬性弱于Z.
點評 本題采取元素推斷形式,考查學生對原子結構、元素周期律、元素周期表、元素化合物以及常用化學用語等知識的掌握和應用能力,關鍵是根據W氫化物性質入手進行推斷.


 每日10分鐘口算心算速算天天練系列答案
每日10分鐘口算心算速算天天練系列答案科目:高中化學 來源: 題型:解答題
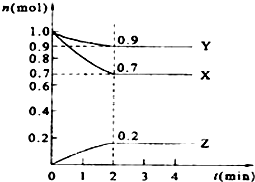 某溫度時,在2L的密閉容器中,X、Y、Z三種物質的量隨時間的變化曲線如圖所示.
某溫度時,在2L的密閉容器中,X、Y、Z三種物質的量隨時間的變化曲線如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 納米級Cu2O由于具有優良的催化性能而受到關注,下表為制取Cu2O的三種方法:
納米級Cu2O由于具有優良的催化性能而受到關注,下表為制取Cu2O的三種方法:| 方法Ⅰ | 用炭粉在高溫條件下還原CuO |
| 方法Ⅱ | 電解法,反應為2Cu+H2O $\frac{\underline{\;電解\;}}{\;}$ Cu2O+H2↑. |
| 方法Ⅲ | 用肼(N2H4)還原新制Cu(OH)2 |
| 序號 | 溫度 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
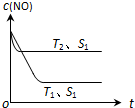 汽車尾氣是城市的主要空氣污染物,研究控制汽車尾氣成為保護環境的首要任務.在汽車上安裝三效催化轉化器,可使汽車尾氣中的主要污染物進行相互反應,生成無毒物質;或者使用新型燃料電池作汽車動力,減少汽車尾氣污染.
汽車尾氣是城市的主要空氣污染物,研究控制汽車尾氣成為保護環境的首要任務.在汽車上安裝三效催化轉化器,可使汽車尾氣中的主要污染物進行相互反應,生成無毒物質;或者使用新型燃料電池作汽車動力,減少汽車尾氣污染.
| 時間/s | 0 | 1 | 2 | 3 | 4 |
| c (NO)(×10-3 mol•L-1) | 1.00 | 0.50 | 0.20 | 0.10 | 0.10 |
| c (CO)(×10-3 mol•L-1) | 3.00 | 2.50 | 2.20 | 2.10 | 2.10 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 10g H2 | B. | 2molCl2 | C. | 1.5NACO2 | D. | 22.4LO2(標準狀況) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該氯原子的相對原子質量為$\frac{a}{b}$ | |
| B. | m g該氯原子的物質的量為$\frac{m}{a{N}_{A}}$mol | |
| C. | 該氯原子的摩爾質量為aNAg | |
| D. | a g該氯原子所含的電子數為17 mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鑒別膠體與濁液(丁達爾效應) | B. | 高壓除塵(電泳現象) | ||
| C. | 河海交匯處可沉積沙洲(聚沉) | D. | 噴霧劑的應用(布朗運動) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
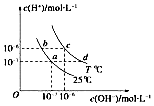
| A. | 若從a點到c點,可采用在水中加入酸的方法 | |
| B. | b點對應的醋酸中由水電離的c(H+)=10-6mol•L-1 | |
| C. | T℃時,0.05 mol•L-1的Ba(OH)2溶液的pH=11 | |
| D. | c點對應溶液的Kw大于d點對應溶液的Kw |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com