
| A. | 若從a點到c點,可采用在水中加入酸的方法 | |
| B. | b點對應的醋酸中由水電離的c(H+)=10-6mol•L-1 | |
| C. | T℃時,0.05 mol•L-1的Ba(OH)2溶液的pH=11 | |
| D. | c點對應溶液的Kw大于d點對應溶液的Kw |
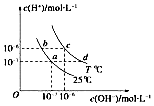
分析 由圖象可知,c、d為T°C的曲線,Kw=10-6×10-6=10-12,a、b都為25℃時的曲線上,Kw=10-7×10-7=10-14,水的Kw只與溫度有關,溫度相同時Kw相同,溫度升高,促進水的電離,Kw增大,T°C大于25°C,另外也可根據c(OH-)×c(H+)計算Kw大小,水的離子積只與溫度有關,與溶液的類型無關,可能為純水,也可能為酸、堿、鹽溶液,
A.a、c點是溫度不同的水溶液,Kw隨溫度變化;
B.b點對應的Kw=10-7×10-7=10-14,醋酸抑制水的電離;
C.T℃時,Kw=10-6×10-6=10-12,據此計算;
D.c、d為T°C的曲線,Kw=10-6×10-6=10-12.
解答 解:A.Kw隨溫度變化,若從a點到c點,需要升高溫度達到,故A錯誤;
B.b點對應的Kw=10-7×10-7=10-14,醋酸抑制水的電離,溶液中由水電離的c(H+)<10-7mol•L-1 ,故B錯誤;
C.T℃時,Kw=10-6×10-6=10-12,0.05 mol•L-1的Ba(OH)2溶液中c(OH-)=0.1mol/L,溶液中氫離子濃度c(H+)=$\frac{1{0}^{-12}}{0.1}$=10-11mol/L,溶液的pH=11,故C正確;
D.c、d為T°C的曲線,溫度不變離子積常數不變,圖象分析可知Kw=10-6×10-6=10-12,故D錯誤;
故選C.
點評 本題考查了水的電離、離子積常數計算和影響因素分析,掌握基礎是解題關鍵,題目難度不大.


科目:高中化學 來源: 題型:推斷題
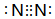 .
. NH3•H2O
NH3•H2O  NH4++OH-.
NH4++OH-.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 物質發生化學變化一定伴隨著能量變化 | |
| B. | 升高溫度或加入催化劑,可以改變化學反應的反應熱 | |
| C. | 據能量守恒定律,反應物的總能量一定等于生成物的總能量 | |
| D. | 熱化學方程式中,如果沒有注明溫度和壓強,則表示反應熱是在標準狀況下測得的 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1.6g 由氧氣和臭氧組成的混合物中含有氧原子的數目為0.1NA | |
| B. | Na2O和Na2O2中陰陽離子個數比都為1:2 | |
| C. | 18g H2O含有10NA個質子 | |
| D. | 標準狀況下,11.2L H2O中含有的分子的數目為0.5 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2-甲基-4-乙基戊烷 | B. | 3,4,4-三甲基己烷 | ||
| C. | 2,3-二乙基-1-戊烯 | D. | 3,4-二甲基-4-乙基己烷 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
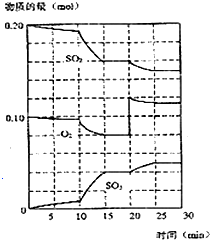 在450℃并有催化劑存在下,于一容積恒定的密閉容器內進行下列反應:2SO2(g)+O2(g)═2SO3(g)△H=-190kJ•mol-1
在450℃并有催化劑存在下,于一容積恒定的密閉容器內進行下列反應:2SO2(g)+O2(g)═2SO3(g)△H=-190kJ•mol-1查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com