
分析 (1)醋酸是弱電解質,向醋酸溶液中加入含有醋酸根離子的物質抑制醋酸電離,醋酸的電離平衡常數只與溫度有關;
(2)99℃時,Kw=1.0×10-12,該溫度下測得0.1mol•L-1 Na2A溶液的pH=6,說明Na2A是強酸強堿鹽;
①H2A是強酸完全電離;
②酸與足量的鋅反應生成氫氣的量與氫離子的物質的量成正比;
(3)物質的溶度積越小,越易形成沉淀.
解答 解:(1)CH3COOH溶液中存在電離平衡CH3COOH?CH3COO-+H+,加入CH3COONa固體,c(CH3COO-)增大,平衡左移;CH3COOH的電離平衡常數K=$\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$,溫度不變,電離平衡常數不變,K的值不變,
故答案為:逆;不變;
(2)99℃時,Kw=1.0×10-12,該溫度下純水的pH=6,測得0.1mol•L-1 Na2A溶液的pH=6,說明Na2A是強酸強堿鹽,
①H2A是強酸,在水溶液里完全電離,其電離方程式為H2A═2H++A2-,
故答案為:H2A═2H++A2-;
②酸與足量的鋅反應生成氫氣的量與氫離子的物質的量成正比,體積相等、pH=2的醋酸與H2A溶液醋酸提供氫離子能力強,所以與足量鋅完全反應時生成的氫氣,醋酸放出的多,故答案為:A;
(3)根據Al(OH)3、Fe(OH)3的溶度積常數,在25℃下,向濃度均為0.1mol•L-1的FeCl3和AlCl3的混合溶液中逐滴加入加入碳酸鈣粉末,$\root{3}{4.0×1{0}^{-38}}<\root{3}{3.0×1{0}^{-34}}$,逐漸加入碳酸鈣粉末,Fe(OH)3最先析出,離子反應方程式為:2Fe3++3H2O+3CaCO3=2Fe(OH)3↓+3Ca2++3CO2,故答案為:Fe(OH)3;2Fe3++3H2O+3CaCO3=2Fe(OH)3↓+3Ca2++3CO2.
點評 本題考查了弱電解質的電離平衡、鹽類水解等知識點,明確弱電解質電離平衡特點及鹽類水解特點是解本題關鍵,易錯點是(2),根據鹽溶液pH確定酸的強弱來分析解答,難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 反應中轉移電子為0.04 mol | B. | Q中n(Cu2+):n(Fe2+)=1:2 | ||
| C. | 溶液Q比原溶液增重了 1.28 g | D. | 3c(Fe3+)+2c(Fe2+)+2c(Cu2+)=0.1 mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A | B | C | D | |
| 氣體 | CO2 | HCl | HCl | SO2 |
| 液體 | H2O | NaOH | H2O | NaOH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
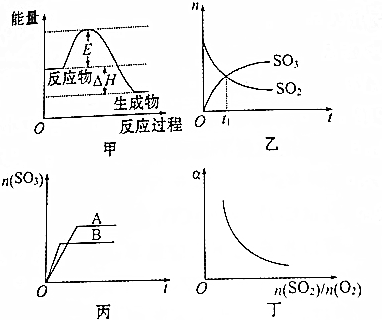
| A. | 加入適當的催化劑后,甲圖中的E和△H都減小 | |
| B. | 乙圖中t1時刻反應達到化學平衡狀態 | |
| C. | 丙圖可以表示其他條件不變時,壓強對反應的影響 | |
| D. | 丁圖中a可以表示SO2的轉化率 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
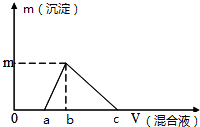 往100mL0.1mol/L NaOH溶液中逐滴滴入濃度均為0.1mol/L的氯化鋁和鹽酸的混合溶液,測得生成沉淀的質量(g)與滴入的混合液的體積(mL)的關系如圖所示,則下列說法正確的是( )
往100mL0.1mol/L NaOH溶液中逐滴滴入濃度均為0.1mol/L的氯化鋁和鹽酸的混合溶液,測得生成沉淀的質量(g)與滴入的混合液的體積(mL)的關系如圖所示,則下列說法正確的是( )| A. | a=25mL | B. | b=33mL | C. | c=100mL | D. | m=0.195g |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.3mol | B. | 0.15mol | C. | 0.1mol | D. | 0.075mol |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
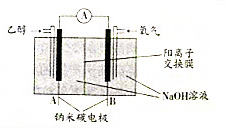
| A. | A極為電池負極,B極為電池正極 | |
| B. | B極的電極反應式為O2+2H2O+4e-═4OH- | |
| C. | 該乙醇燃料電池的總反應方程式為:C2H5OH+3O2═2CO2+3H2O | |
| D. | 當電池消耗4.6g乙醇時,經過陰離子交換膜的OH-為1.2mol |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com