
| A、2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | B、2Fe3++H2S═2Fe2++S+2H+ | C、I2+SO2+2H2O═2I-+SO42-+4H+ | D、2Br-+SO42-+4H+═Br2+SO2+2H2O |
科目:高中化學 來源: 題型:閱讀理解
 水合肼作為一種重要的精細化工原料,在農藥、醫藥及有機合成中有廣泛用途. 用尿素法制備水合肼,可分為兩個階段,第一階段為低溫氯化階段,第二階段為高溫水解階段,總反應方程式為:(NH2)2CO+NaClO+2NaOH→H2N-NH2?H2O+NaCl+Na2CO3.
水合肼作為一種重要的精細化工原料,在農藥、醫藥及有機合成中有廣泛用途. 用尿素法制備水合肼,可分為兩個階段,第一階段為低溫氯化階段,第二階段為高溫水解階段,總反應方程式為:(NH2)2CO+NaClO+2NaOH→H2N-NH2?H2O+NaCl+Na2CO3.查看答案和解析>>
科目:高中化學 來源:高一化學(通用各科奧林匹克ABC卷及解析) 題型:013
在一定條件下,還原性順序為:![]() <
<![]() <
<![]() <
<![]() <
<![]() <
<![]() ,由此判斷下列反應不能發生的是
,由此判斷下列反應不能發生的是
[ ]
A.![]()
B.![]()
C.![]()
D.![]()
查看答案和解析>>
科目:高中化學 來源:2013屆江蘇省南京學大教育專修學校高三4月月考化學試卷(帶解析) 題型:實驗題
水合肼作為一種重要的精細化工原料,在農藥、醫藥及有機合成中有廣泛用途。用尿素法制備水合肼,可分為兩個階段,第一階段為低溫氯化階段,第二階段為高溫水解階段,總反應方程式為:(NH2)2CO +NaClO+2NaOH → H2N—NH2·H2O+NaCl+Na2CO3。
主要副反應:N2H4+2NaClO= N2↑+2H2O+2NaCl △H<0
3NaClO=" 2NaCl" +NaClO3 △H>0
CO(NH2)2 +2NaOH= 2NH3↑+Na2CO3 △H>0
【深度氧化】:(NH2)2CO+3NaClO= N2↑+3NaCl+CO2↑+2H2O △H<0
實驗步驟:
步驟1.向30%的NaOH溶液中通入Cl2,保持溫度在30℃以下,至溶液顯淺黃綠色停止通Cl2。
步驟2.靜置后取上層清液,檢測NaClO的濃度。
步驟3.傾出上層清液,配制所需濃度的NaClO和NaOH的混合溶液。
步驟4.稱取一定質量尿素配成溶液,置于冰水浴。將一定體積步驟3配得的溶液倒入分液漏斗中,慢慢滴加到尿素溶液中,0.5h左右滴完后,繼續攪拌0.5h。
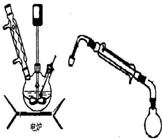
步驟5.將步驟4所得溶液,加入5g KMnO4作催化劑,轉移到三口燒瓶(裝置見圖),邊攪拌邊急速升溫,在108℃回流5 min。
步驟6.將回流管換成冷凝管,蒸餾,收集( 108~114℃)餾分,得產品。
(1)步驟1溫度需要在30℃以下,其主要目的是 。
(2)步驟2檢測NaClO濃度的目的是 。
a.確定步驟3中需NaClO溶液體積及NaOH質量
b.確定步驟4中冰水浴的溫度范圍
c.確定步驟4中稱量尿素的質量及所取次氯酸鈉溶液體積關系
d.確定步驟5所需的回流時間
(3)尿素法制備水合肼,第一階段為反應 (選填:“放熱”或“吸熱”)。
(4)步驟5必須急速升溫,嚴格控制回流時間,其目的是 。
(5)已知水合肼在堿性條件下具有還原性(如:N2H4+2I2=N2+4HI)。測定水合肼的質量分數可采用下列步驟:
a.準確稱取2.000g試樣,經溶解、轉移、定容等步驟,配制250mL溶液。
b.移取l0.00 mL于錐形瓶中,加入20mL水,搖勻.
c.用0.l000 mol/L碘溶液滴定至溶液出現微黃色且Imin內不消失,計錄消耗碘的標準液的體積。
d.進一步操作與數據處理
①滴定時,碘的標準溶液盛放在 滴定管中(選填:“酸式”或“堿式”)。
②若本次滴定消耗碘的標準溶液為18.00mL,可測算出產品中N2H4-H2O的質量分數為 。
③為獲得更可靠的滴定結果,步驟d中進一步操作主要是:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com