
分析 反應后固體有剩余,加熱發生Fe+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$FeSO4+2H2O+SO2↑,n(氣體)=$\frac{4.48L}{22.4L/mol}$=0.2mol,若氣體為二氧化硫其質量為0.2mol×64g/mol=12.8g>6.6g,則還發生Fe+H2SO4(稀)$\frac{\underline{\;\;△\;\;}}{\;}$FeSO4+H2↑,結合物質的量關系及質量關系計算.
解答 解:反應后固體有剩余,加熱發生Fe+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$FeSO4+2H2O+SO2↑,n(氣體)=$\frac{4.48L}{22.4L/mol}$=0.2mol,若氣體為二氧化硫其質量為0.2mol×64g/mol=12.8g>6.6g,則還發生Fe+H2SO4(稀)$\frac{\underline{\;\;△\;\;}}{\;}$FeSO4+H2↑,
設二氧化硫、氫氣的物質的量分別為x、y,則
$\left\{\begin{array}{l}{x+y=0.2}\\{64x+2y=6.6}\end{array}\right.$
解得x=0.1mol,y=0.1mol,
(1)由反應可知,n(Fe)=n(SO2)+n(H2)=0.2mol,其質量為0.2mol×56g/mol=11.2 g,故答案為:11.2 g;
(2)由反應可知,n(H2SO4)=2n(SO2)+n(H2)=0.3mol,則硫酸溶液的物質的量濃度為$\frac{0.3mol}{0.02L}$=15 mol/L,故答案為:15 mol/L.
點評 本題考查氧化還原反應的計算,為高頻考點,把握發生的反應及物質的、質量關系為解答的關鍵,側重分析與計算能力的考查,題目難度不大.


 津橋教育計算小狀元系列答案
津橋教育計算小狀元系列答案科目:高中化學 來源: 題型:選擇題
| A. | 斷開1個N≡N鍵的同時有6個N-H鍵生成 | |
| B. | 混合氣體的密度不變 | |
| C. | 混合氣體的平均相對分子質量不變 | |
| D. | N2、H2、NH3分子數之比為1:3:2的狀態 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2SO4→MgSO4 | B. | NaCl→Cl2 | C. | CuSO4→Cu | D. | HClO→Cl2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
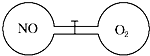 一定溫度下,兩個體積相等的連通容器用活塞分開,左右兩室各充入一定量NO和O2,恰好使兩容器內氣體密度相同,打開活塞,充分混合反應.下列判斷正確的是(不考慮NO2轉化為N2O4)( )
一定溫度下,兩個體積相等的連通容器用活塞分開,左右兩室各充入一定量NO和O2,恰好使兩容器內氣體密度相同,打開活塞,充分混合反應.下列判斷正確的是(不考慮NO2轉化為N2O4)( )| A. | 最終容器內無O2存在 | B. | 反應前、后左室氣體壓強不變 | ||
| C. | 反應前、后右室氣體密度不變 | D. | 開始時左右兩室氣體分子數相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH2O和CO2分子中的中心原子均采用sp2雜化 | |
| B. | CH3SH 的相對分子質量比CH3OH大,因此前者的沸點高 | |
| C. | C6H6分子中含有6個σ鍵和1個大π鍵,C6H6是非極性分子 | |
| D. | 甲胺(分子式CH3NH2)的沸點比三甲胺[分子式(CH3)3N]的沸點高 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. |  如圖一個超氧化鉀小晶胞中含有4個KO2 | |
| B. | 和K+距離相同且最近的O2-構成的多面體是正六面體 | |
| C. | 和K+距離相同且最近的K+有8個 | |
| D. | 和K+距離相同且最近的O2-共有8個 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用溴水或酸性KMnO4溶液鑒別甲烷和乙烯 | |
| B. | 向酒精中加入足量生石灰檢驗酒精中是否含有少量水 | |
| C. | 在盛有2mL無水乙醇的試管中放入繞成螺旋狀的光潔銅絲,加熱可制得乙醛 | |
| D. | 將裂解氣通入到酸性KMnO4溶液中來證明裂解氣中是否有乙烯 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2~4 s內的平均反應速率為0.2 mol•L-1•s-1 | |
| B. | 前4 s內的平均反應速率為0.3 mol•L-1•s-1 | |
| C. | 前2 s內的平均反應速率為0.4 mol•L-1•s-1 | |
| D. | 2 s末的反應速率為0.4 mol•L-1•s-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com