
| 實驗編號 | HA的物質的量 濃度(mol•L-1) | NaOH的物質的量 濃度(mol•L-1) | 混合后 溶液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.12 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=10 |
分析 (1)等物質的量混合時,二者恰好反應生成鹽,根據溶液的pH判斷酸性強弱;
(2)酸堿混合時,酸過量,而溶液顯中性,說明酸為弱酸,溶液中溶質為HA、NaA;
(3)混合溶液的溶質為等物質的量的HA和NaA,pH>7說明A-的水解大于HA的電離,結合電荷守恒判斷;
(4)由電荷守恒關系式變形得c(Na+)-c(A-)=c(OH-)-c(H+);
(5)等物質的量反應生成NaA,溶液顯堿性,則NaA發生水解.
解答 解:(1)若HA是強酸,恰好與NaOH溶液反應生成強酸強堿鹽,pH=7;若HA是弱酸,生成的NaA水解顯堿性,pH>7,所以不能判斷HA的酸性強弱;
故答案為:不能;
(2)酸堿混合時,酸過量,而溶液顯中性,說明酸為弱酸,溶液中溶質為HA、NaA,溶液中存在HA的電離平衡,NaA的水解平衡,水的電離平衡;
故答案為:3;
(3)混合溶液的溶質為等物質的量的HA和NaA,pH>7,說明A-的水解大于HA的電離,所以離子濃度由大到小的順序為c(Na+)>c(A-)>c(OH-)>c(H+);
故答案為:c(Na+)>c(A-)>c(OH-)>c(H+);
(4)由電荷守恒關系式變形得c(Na+)-c(A-)=c(OH-)-c(H+)=(10-4-10-10)mol•L-1,
故答案為:10-4-10-10;
(5)等物質的量反應生成NaA,溶液顯堿性,則NaA發生水解,其水解方程式為:A-+H2O?HA+OH-;
故答案為:A-+H2O?HA+OH-.
點評 本題考查了弱電解質的電離、離子濃度大小的比較,題目難度中等,明確弱電解質電離特點結合物料守恒、電荷守恒和質子守恒來分析解答解答,側重于考查學生的分析能力和對基礎知識的應用能力.


 名師金手指領銜課時系列答案
名師金手指領銜課時系列答案科目:高中化學 來源: 題型:選擇題
| A. | 1:9 | B. | 9:1 | C. | 10:1 | D. | 1:10 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
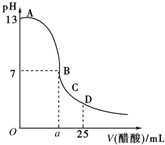 25℃時,在25mL 0.1mol/L的NaOH溶液中,逐滴加入0.2mol/L的CH3COOH溶液,溶液的pH變化如下圖所示,下列分析的結論中正確的是( )
25℃時,在25mL 0.1mol/L的NaOH溶液中,逐滴加入0.2mol/L的CH3COOH溶液,溶液的pH變化如下圖所示,下列分析的結論中正確的是( )| A. | B點的橫坐標a=12.5 | |
| B. | C點時溶液中有:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| C. | D點時溶液中有:c(CH3COO-)+c(CH3COOH)=2c(Na+) | |
| D. | 曲線上A、B間的任意一點,溶液中都有:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
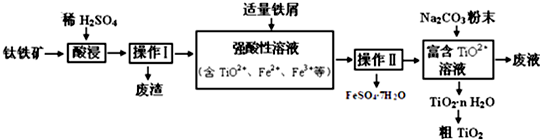
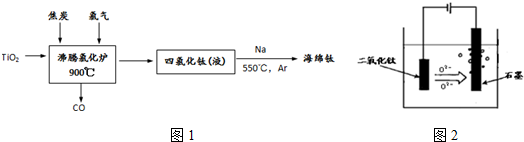
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④ | B. | ②⑥ | C. | ③④ | D. | ②⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
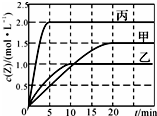 向甲、乙、丙三個容積固定不變的密閉容器中充入一定量的X和Y,一定條件下發生反應 X(g)+aY(g)?2Z(g).各容器的反應溫度、反應物起始量、反應過程中Z的濃度隨時間變化分別以如圖和下表來表示.下列說法不正確的是( )
向甲、乙、丙三個容積固定不變的密閉容器中充入一定量的X和Y,一定條件下發生反應 X(g)+aY(g)?2Z(g).各容器的反應溫度、反應物起始量、反應過程中Z的濃度隨時間變化分別以如圖和下表來表示.下列說法不正確的是( ) | 容器 | 甲 | 乙 | 丙 | |
| 容積/L | 0.5 | 0.5 | 1.0 | |
| 溫度/℃ | T1 | T2 | T2 | |
| 反應物起始量 | 1.0 mol X 0.5 mol Y | 1.0 mol X 0.5 mol Y | 4.0 mol X 2.0 mol Y |
| A. | 該反應溫度升高,平衡常數減小 | |
| B. | 20 min內甲容器中反應的平均速率:v(X)=0.0375mol•(L•min)-1 | |
| C. | 10 min時,其他條件不變,向乙容器中再加入2 mol Z,平衡向逆反應方向移動 | |
| D. | 其他條件不變,若縮小乙的體積,Y的轉化率增大 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com