
 某研究小組探究:
某研究小組探究:分析 (1)①加熱條件下,Cu和濃硫酸反應生成硫酸銅、二氧化硫和水;
②測定SO2的量必須做到不能在測量時損耗,便于測定分析,堿石灰能吸收二氧化硫和水,二氧化硫易溶于水;
(2)為排除空氣對實驗的干擾,滴加濃硫酸之前應先通入氮氣,將空氣排出;
(3)Fe3+和酸性條件下NO3-兩種離子都氧化二氧化硫,可根據反應產物進行判斷;
①按猜想1,裝置B中反應的離子方程式是SO2+2Fe3++Ba2++2H2O=BaSO4↓+2Fe2++4H+,可通過檢驗是否有Fe2+生成的方法判斷;
②根據硝酸根離子守恒的方法分析解答.
解答 解:(1)①裝置A中反應的化學方程式是Cu+2H2S04(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuS04+SO2↑+2H2O,故答案為:Cu+2H2S04(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuS04+SO2↑+2H2O;
②A.將裝置產生的氣體緩緩通過預先稱量過盛有堿石灰的干燥管,結束反應后再次稱量,由于氣體中含有水蒸氣,堿石灰會吸收二氧化硫和水蒸氣,稱量后計算不準確,故A錯誤;
B.二氧化硫具有還原性,與酸性髙錳酸鉀溶液發生氧化還原生成硫酸鹽,再加入足量BaCl2溶液,可通過測量所得沉淀的質量進行二氧化硫的氣體體積測定,故B正確;
C.二氧化硫易溶于水,計算不準確,故C錯誤;
D.用排飽和NaHSO3溶液的方法測出裝置A產生氣體的體積,二氧化硫在飽和NaHSO3溶液中的溶解度降低,可以用排水量氣方法進行二氧化硫的氣體體積測定,故D正確;
故答案為:AC;
(2)為排除空氣對實驗的干擾,滴加濃硫酸之前應先通入氮氣,將空氣排出,操作為打開彈簧夾,向裝置中通入一段時間的N2,關閉彈簧夾,
故答案為:打開彈簧夾,向裝置中通入一段時間的N2,關閉彈簧夾;
(3)猜想3:兩種離子都氧化二氧化硫,即SO2和Fe3+、酸性條件下NO3-都反應,故答案為:SO2和Fe3+、酸性條件下NO3-都反應;
①按猜想1,裝置B中反應的離子方程式是SO2+2Fe3++Ba2++2H2O=BaSO4↓+2Fe2++4H+,可通過檢驗是否有Fe2+生成的方法判斷,具體做法為取少量B中溶液于試管中,加入少量鐵氰化鉀[K3Fe(CN)6]溶液產生藍色沉淀,則溶液中有Fe2+,猜想1合理,
故答案為:SO2+2Fe3++Ba2++2H2O=BaSO4↓+2Fe2++4H+;取少量B中溶液于試管中,加入少量鐵氰化鉀[K3Fe(CN)6]溶液產生藍色沉淀,則溶液中有Fe2+;
②按猜想2,在酸性條件下SO2與NO3-反應,實驗中c(NO3-)=3mol/L,則可用6.0mol•L-1NaNO3和0.2mol•L-1鹽酸等體積混合的溶液代替,但b中亞鐵離子具還原性,而猜想2是酸性條件下SO2與N03?反應,干擾該猜想的驗證,故選c.
點評 本題考查物質的性質實驗探究,題目難度中等,注意把握物質的性質,為解答該題的關鍵,學習中注意相關知識的積累.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:多選題
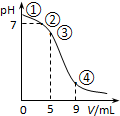 25℃時,向10mL 0.1mol•L-1 CH3COONa溶液中加入0.1mol•L-1鹽酸,溶液pH隨加入鹽酸的體積變化情況如圖所示.下列說法正確的是( )
25℃時,向10mL 0.1mol•L-1 CH3COONa溶液中加入0.1mol•L-1鹽酸,溶液pH隨加入鹽酸的體積變化情況如圖所示.下列說法正確的是( )| A. | 點①所示溶液中:c(OH-)=c(H+)+c(CH3COOH) | |
| B. | 點②所示溶液中:c(CH3COOH)+c(CH3COO-)=0.05 mol•L-1 | |
| C. | 點③所示溶液中:c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) | |
| D. | 點④所示溶液中:c(Na+)+c(H+)<c(CH3COO-)+c(Cl-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH2O與C2H4O2 | B. | C4H10與C4H6O | C. | CF2Cl2與C2F2Cl2 | D. | C4H10與C3H6 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 ,下列相關說法中不正確的是( )
,下列相關說法中不正確的是( )| A. | 一定條件下能發生酯化反應 | |
| B. | 一定條件下能發生催化氧化反應 | |
| C. | 不能發生加成反應 | |
| D. | 1mol該物質與Na2CO3溶液反應最多消耗1.5mol Na2CO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
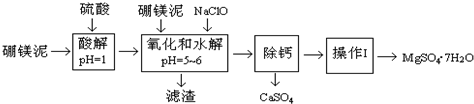
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 |
| 開始沉淀pH | 2.3 | 4.0 | 7.6 |
| 完全沉淀pH | 4.1 | 5.2 | 9.6 |
| 溫度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 物質 | 性質(沸點及分解溫度均為101kPa測得) |
| 鄰苯二甲酸酐 (M=148g/mol) | 白色針狀晶體.不溶于冷水,溶于熱水及有機溶劑. 密度1.53g/cm3,沸點295℃. |
| 正丁醇(M=74g/mol) | 無色液體.微溶于水,溶于有機溶劑.密度0.81g/cm3,沸點117.7℃.可與水形成二元共沸物(沸點92.7℃). |
| 鄰苯二甲酸二丁酯 (M=278g/mol) | 無色油狀液體.難溶于水,溶于有機溶劑.密度1.49g/cm3,沸點340℃.酸性條件下180℃以上易發生分解. |
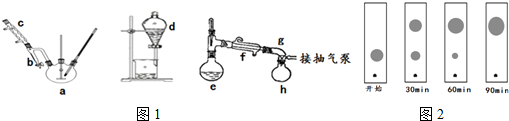
 轉變成鹽,從而與產物分離,該操作是否可改用NaOH溶液?否(填“是”或“否”),原因是;氫氧化鈉堿性太強,能使鄰苯二甲酸二丁酯發生水解;.加入食鹽水洗滌一方面是防止有機物發生乳化而不利于分層,另一方面是為了降低鄰苯二甲酸二丁酯的溶解度.
轉變成鹽,從而與產物分離,該操作是否可改用NaOH溶液?否(填“是”或“否”),原因是;氫氧化鈉堿性太強,能使鄰苯二甲酸二丁酯發生水解;.加入食鹽水洗滌一方面是防止有機物發生乳化而不利于分層,另一方面是為了降低鄰苯二甲酸二丁酯的溶解度.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

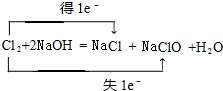 ;
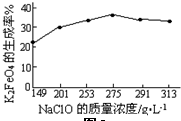
;
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
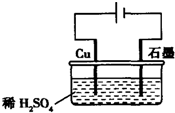
| A. | 電解過程中,銅電極上有H2產生 | |
| B. | 電解初期,主要反應方程式為:Cu+H2SO4$\frac{\underline{\;電解\;}}{\;}$CuSO4+H2↑ | |
| C. | 電解一定時間后,石墨電極上有銅析出 | |
| D. | 整個電解過程中,H+的濃度不斷增大 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com