
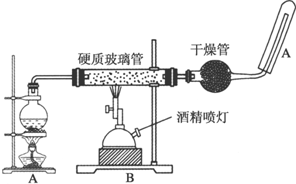
分析 A中圓度燒瓶在加熱條件下可提供水蒸氣,B在加熱條件下,鐵與水蒸氣反應生成四氧化三鐵和氫氣,氫氣經干燥,在試管中用向下排空法可收集到氫氣,可用KSCN檢驗鐵離子,氫氣密度比空氣小,可用KSCN檢驗鐵離子,以此解答該題.
解答 解:(1)Fe與水蒸氣反應生成四氧化三鐵和氫氣,該反應為,Fe元素的化合價升高,Fe為還原性,H元素的化合價降低,則水為氧化劑,
故答案為:3Fe+4H2O(g)$\frac{\underline{\;高溫\;}}{\;}$Fe3O4+4H2;H2O;
(2)實驗前必須對整套裝置進行氣密性檢查,故答案為:檢驗裝置的氣密性;
(3)因為反應物為水蒸氣與鐵,所以這里加熱的目的就是提供水蒸氣;碎瓷片可防止暴沸發生,故答案為:提供持續不斷的水蒸氣;防止暴沸;
(4)檢驗鐵離子,可加入KSCN,發生絡合反應,溶液變為血紅色,故答案為:KSCN;溶液變為血紅色.
點評 本題考查了鐵及其化合物的性質實驗,題目難度不大,注意掌握鐵與水蒸氣反應原理,試題側重對學生能力的培養和訓練,有利于培養學生規范嚴謹的實驗設計、操作能力.


科目:高中化學 來源: 題型:選擇題
| A. | 7.8gNa2O2含有的共價鍵數為0.2NA | |
| B. | 7.8gNa2S與Na2O2的混合物,含離子總數為0.3NA | |
| C. | 標準狀況下,22.4L溴單質含有NA個溴分子 | |
| D. | 0.2 molNa被完全氧化生成7.8gNa2O2,轉移電子的數目為0.4NA |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 可用圖示裝置制取少量乙酸乙酯(酒精燈等在圖中均已略去).請填空:
可用圖示裝置制取少量乙酸乙酯(酒精燈等在圖中均已略去).請填空:查看答案和解析>>
科目:高中化學 來源: 題型:填空題
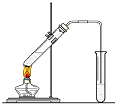 在實驗室我們用如圖所示的裝置制取乙酸乙酯.回答下列問題:
在實驗室我們用如圖所示的裝置制取乙酸乙酯.回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:填空題
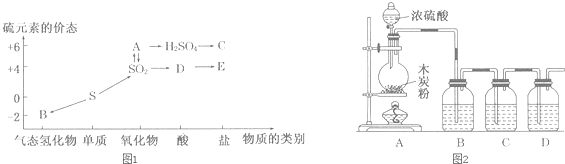
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
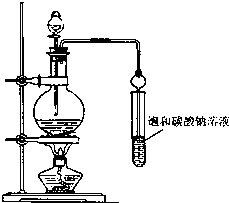 實驗室合成乙酸乙酯粗產品的步驟如下:在蒸餾燒瓶內將過量的乙醇和少量濃H2SO4混合,然后經分液漏斗邊滴加醋酸,邊加熱蒸餾,直接收集蒸餾產品可得到含有乙醇、乙醚、醋酸、少量水的乙酸乙酯粗產品.據此回答問題:
實驗室合成乙酸乙酯粗產品的步驟如下:在蒸餾燒瓶內將過量的乙醇和少量濃H2SO4混合,然后經分液漏斗邊滴加醋酸,邊加熱蒸餾,直接收集蒸餾產品可得到含有乙醇、乙醚、醋酸、少量水的乙酸乙酯粗產品.據此回答問題: CH3COOC2H5+H2O.
CH3COOC2H5+H2O.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| 乙醇 | 溴乙烷 | 溴 | |
| 狀態 | 無色液體 | 無色液體 | 深紅棕色液體 |
| 密度/g•cm-3 | 0.79 | 1.44 | 3.1 |
| 沸點/℃ | 78.5 | 38.4 | 59 |
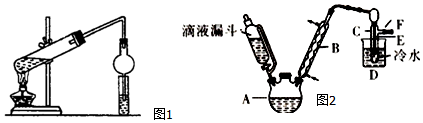
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
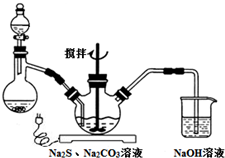 NaCN為劇毒無機物.某興趣小組查資料得知,實驗室里的NaCN溶液可用Na2S2O3溶液進行解毒銷毀,他們開展了以下三個實驗,請根據要求回答問題:
NaCN為劇毒無機物.某興趣小組查資料得知,實驗室里的NaCN溶液可用Na2S2O3溶液進行解毒銷毀,他們開展了以下三個實驗,請根據要求回答問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com