
 如表為元素周期表短周期的一部分.回答下列問題:
如表為元素周期表短周期的一部分.回答下列問題:分析 由元素在短周期中的位置,可知A為碳元素、B為O元素、C為F元素、D為S元素、E為Cl.
(1)碳元素與氧元素可以形成碳酸根、草酸根;
(2)HF分子之間存在氫鍵,沸點高于HCl;
(3)硫在氧氣中燃燒生成二氧化硫;非金屬性越強,最高價含氧酸的酸性越強.
解答 解:由元素在短周期中的位置,可知A為碳元素、B為O元素、C為F元素、D為S元素、E為Cl.
(1)碳元素與氧元素可以形成CO32-、C2O42-,故答案為:CO32-、C2O42-;
(2)HF分子之間存在氫鍵,HCl分子之間為范德華力,故沸點HF>HCl,故答案為:低;HF分子間存在氫鍵;
(3)硫在氧氣中燃燒生成二氧化硫,反應方程式為S+O2$\frac{\underline{\;點燃\;}}{\;}$SO2;非金屬性Cl>S,非金屬性越強,最高價含氧酸的酸性越強,故酸性:HClO4>H2SO4,
故答案為:S+O2$\frac{\underline{\;點燃\;}}{\;}$SO2; HClO4>H2SO4.
點評 本題考查元素周期表與元素周期律,比較基礎,注意對元素周期表的理解掌握.


科目:高中化學 來源: 題型:選擇題
| A. | 鋅是正極,氧化銀是負極 | |
| B. | 鋅發生還原反應,氧化銀發生氧化反應 | |
| C. | 溶液中OH-向正極移動,K+、H+向負極移動 | |
| D. | 隨著電極反應的不斷進行,電解質溶液中KOH的質量分數不斷增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子最外層電子數:X>Y>Z | B. | 單質活潑性:X>Y>Z | ||
| C. | 原子序數:X>Y>Z | D. | 離子半徑:X2->Y+>Z- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4LNO和11.2LO2混合后氣體的分子總數為1.5NA | |
| B. | 6.2gNa2O和7.8gNa2O2混合物中所含有的陰離子數為0.3 NA | |
| C. | 14g乙烯和丙烯的混合物中,含有共用電子對數目為3×6.02×1023 | |
| D. | 18g D2O(重水)完全電解,轉移6.02×1023個電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
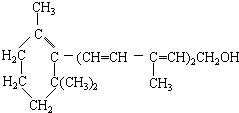
| A. | 維生素A分子含有氫原子數為奇數 | |
| B. | 維生素A的分子中含有苯環結構 | |
| C. | 1mol維生素A在催化劑作用下,可以和5molH2完全加成 | |
| D. | 維生素A屬于醇,是一種水溶性維生素,可以發生消去反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
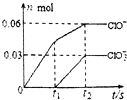 將一定量的Cl2通入一定濃度的苛性鉀溶液中,兩者恰好完全反應(已知反應過程放熱),生成物中有三種含氯元素的離子,其中ClO-和ClO${\;}_{3}^{-}$兩種離子的物質的量(n)與反應時間(t)的變化示意圖如圖所示.下列說法正確的是( )
將一定量的Cl2通入一定濃度的苛性鉀溶液中,兩者恰好完全反應(已知反應過程放熱),生成物中有三種含氯元素的離子,其中ClO-和ClO${\;}_{3}^{-}$兩種離子的物質的量(n)與反應時間(t)的變化示意圖如圖所示.下列說法正確的是( )| A. | 苛性鉀溶液中KOH的質量是4.94g | |
| B. | 反應中轉移電子的物質的量是0.21mol | |
| C. | Cl-的物質的量為0.09mol | |
| D. | ClO${\;}_{3}^{-}$的生成是由于KOH過量引起的 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 醋酸溶液的pH=a,將此溶液稀釋1倍后,溶液的pH=b,則a>b | |
| B. | 在滴有酚酞溶液的氨水里,加入NH4C1至溶液恰好無色,則此時溶液的pH<7 | |
| C. | 物質的量濃度相等的CH3COOH和CH3COONa溶液等體積混合,c(CH3COO-)+2c(OH-)═2c(H+)+c(CH3COOH) | |
| D. | pH=5.6的CH3COOH與CH3COONa混合溶液中,c(CH3COO-)<c(Na+) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 由Al、Cu、稀H2SO4組成原電池,其負極反應式為:Al-3e-=Al3+ | |
| B. | 由Mg、Al、NaOH溶液組成原電池,其負極反應式為:Al-3e-+3OHˉ=Al(OH)3 | |
| C. | 由Fe、Cu、FeCl3溶液組成原電池,其負極反應式為:Fe-2e-=Fe2+ | |
| D. | 由Fe、Cu、濃硝酸組成的原電池,開始時其負極反應式為:Cu-2e-=Cu2+ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com