
分析 (1)根據構造原理書寫出基態鍺原子核外電子排布式;
(2)①原子核外沒有兩個運動狀態完全相同的電子,有幾個電子就有幾種運動狀態;
②元素的非金屬性越強,其電負性越大;
③根據價層電子對互斥理論確定雜化和離子空間構型,陰陽離子之間存在離子鍵,非金屬元素之間存在共價鍵,含有孤電子對的原子和含有空軌道的原子之間存在配位鍵;
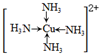
(3)配位數:中心原子周圍的配位原子個數;該配合物的配離子中Cu原子和N原子、氨氣分子中N原子和H原子之間都存在σ鍵;銅離子與氨分子中的氮形成配位鍵;
(4)同一周期元素中,元素的第一電離能隨著原子序數增大而呈增大趨勢,但第IIA族、第VA族元素第一電離能大于其相鄰元素.
解答 解:(1)鍺為32號元素,根據構造原理書,基態鍺原子核外電子排布式:1s22s22p63s23p63d104s24p2或[Ar]3d104s24p2,
故答案為:1s22s22p63s23p63d104s24p2或[Ar]3d104s24p2;
(2)①Ti原子核外有22個電子,所以有22種不同運動狀態的電子,
故答案為:22;
②非金屬的非金屬性越強其電負性越大,非金屬性最強的是H元素,其次是B元素,最小的是Li元素,所以Li、B、H元素的電負性由大到小排列順序為H>B>Li,
故答案為:H>B>Li;
③BH4-中B原子價層電子數=4+$\frac{1}{2}$=4,所以為SP3雜化,且不含孤電子對,是正四面體構型,Li+和BH-4之間存在離子鍵,硼原子和氫原子之間存在共價鍵、配位鍵,所以該化合物中不含金屬鍵,
故答案為:正四面體;SP3雜化;C;
(3)[Cu(NH3)4]Cl2中Cu2+與NH3形成4個配位鍵,所以該配合物的配位數是4,NH3中含有3個N-H鍵,均為σ鍵,故1mol[Cu(NH3)4]Cl2含有(4+3×4)mol=16molσ鍵,則含有σ鍵的數目為16NA,銅離子有空軌道,氨氣分子有孤對電子,銅離子與氨分子中的氮形成配位鍵,所以配離子[Cu(NH3)4]2+的結構簡式為: ,
,
故答案為:4,16NA; ;
;
(4)鎂、鋁屬于同一周期元素,鎂的價電子排布是3s2,3p軌道全空較穩定,而鋁是3s23p1則不是全滿,全空,半空中任意一種情況,不穩定,故鋁的第一電離能比鎂小,
故答案為:Mg的3P軌道為全空狀態,而Al的3P軌道為3P1,不是全空,全滿或半滿狀態.
點評 本題考查物質結構和性質,涉及核外電子排布、雜化方式的判斷、空間構型的判斷、配合物、第一電離能大小比較等知識點,易錯點是鎂、鋁第一電離能大小比較,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 在堿性溶液中:Na+、NH4-、Cl-、NO3- | |
| B. | pH=4的無色溶液中:Na+、Ba2+、Cl-、SO32- | |
| C. | pH=10的無色溶液中:H+、NH4-、HCO3-、Cl- | |
| D. | 中性溶液中:K+、Na+、NO3-、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 葡萄糖注射液不能產生丁達爾效應,不屬于膠體 | |
| B. | 油脂是高分子化臺物,水解可生成甘油和高級脂肪酸 | |
| C. | 煤中含有的煤焦油,可由煤干餾獲得 | |
| D. | 聚乙烯塑料的老化是因為發生了加成反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na和O2 | B. | Fe和稀HNO3 | C. | Cu和FeCl3溶液 | D. | Na2CO3和稀HCl |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
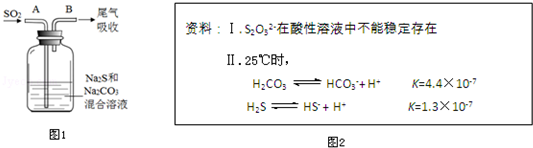
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 在實驗室里制取乙烯的反應為:
在實驗室里制取乙烯的反應為: $→_{170℃}^{濃硫酸}$CH2=CH2↑+H2O
$→_{170℃}^{濃硫酸}$CH2=CH2↑+H2O .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
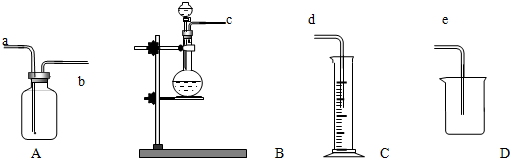
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
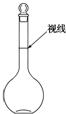 實驗室配制500mL 0.2mol•L-1的Na2SO4溶液,實驗操作步驟有:
實驗室配制500mL 0.2mol•L-1的Na2SO4溶液,實驗操作步驟有:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com