
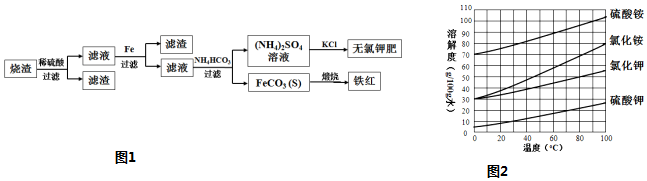
分析 Fe2O3、Fe3O4、FeO用稀硫酸溶解,再用鐵還原生成硫酸亞鐵溶液,硫酸亞鐵溶液與碳酸氫銨反應得到碳酸亞鐵和硫酸銨,實驗室進行煅燒得鐵紅;根據硫酸鉀的溶解度隨溫度變化不大,可用蒸發結晶、趁熱過濾、洗滌、干燥得到硫酸鉀,
(1)根據在化合物中正負化合價代數和為零,四氧化三鐵為黑色氧化物,但可被磁鐵吸引,所以具有磁性,鐵紅的主要成分是氧化鐵,可作顏料、煉鐵等用;
(2)濾液中為硫酸亞鐵、硫酸鐵、硫酸,則濾液中加入鐵粉與Fe3+反應;檢驗Fe3+的試劑是KSCN;
(3)根據硫酸鉀的溶解度隨溫度變化不大,加入KCl后得到無氯鉀肥應進行的操作為蒸發濃縮、趁熱過濾、洗滌、干燥得到硫酸鉀,趁熱過濾的目的是防止氯化銨析出得到無氯鉀肥;過濾操作的玻璃儀器有燒杯、玻璃棒、漏斗.
解答 解:(1)硫顯負價時,顯-2價,根據在化合物中正負化合價代數和為零可知,FeS中,鐵元素的化合價為+2價;四氧化三鐵為黑色氧化物,但可被磁鐵吸引,所以具有磁性,鐵紅的主要成分是Fe2O3,可作顏料、煉鐵等用,
故答案為:+2;Fe3O4;顏料;
(2)濾液中為硫酸亞鐵、硫酸鐵、硫酸,則濾液中加入鐵粉與Fe3+反應;2Fe3++Fe=3Fe2+;檢驗Fe3+的試劑是KSCN;
故答案為:2Fe3++Fe=3Fe2+;KSCN;
(3)根據硫酸鉀的溶解度隨溫度變化不大,加入KCl后得到無氯鉀肥應進行的操作為蒸發濃縮、趁熱過濾、洗滌、干燥得到硫酸鉀\,趁熱過濾的目的是防止氯化銨析出得到無氯鉀肥;過濾操作的玻璃儀器有燒杯、玻璃棒、漏斗.
故答案為:防止析出氯化銨;漏斗.
點評 本題綜合考查物質的分離、提純以及制備,為高考常見題型,側重于學生的分析能力和實驗能力的考查,注意把握實驗原理的分析,難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 分子個數比為4:5 | B. | 含硫元素質量比為4:5 | ||
| C. | 含氧原子個數比為5:6 | D. | 含硫原子個數比為5:6 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | c(H+)>c(OH-) | B. | c(H+)<c(OH-) | ||
| C. | c(H+)+c(HCN)=c(OH-) | D. | c(HCN)+c(CN-)=0.01mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 只含Fe2+ | B. | 只含Cu2+、Fe2+ | ||
| C. | 只含Fe3+、Fe2+ | D. | 只含Fe3+、Cu2+、Fe2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗操作 | 實驗目的 |
| A | 將少量硫酸鋁溶液滴入氫氧化鈉中 | 制備氫氧化鋁 |
| B | 向碘化亞鐵溶液中滴加酸化的雙氧水 | 驗證:氧化性H2O2>Fe3+ |
| C | 向CH2=CHCH2OH中滴加酸性重絡酸鉀溶液 | 證明有機物中含有羥基 |
| D | 室溫下,測定0.1mol•L-1NaX、NaY溶液的pH | 探究HX、HY的電離常數大小 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 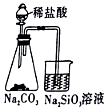 如圖,可以證明非金屬性強弱:Cl>C>Si | |
| B. | 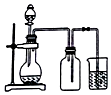 如圖,用銅片和稀硝酸制NO | |
| C. | 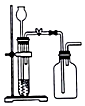 如圖,用鋅粒和稀硫酸制H2 | |
| D. | 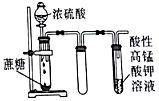 如圖,酸性KMnO4溶液中有氣泡出現,且溶液顏色會逐漸變淺乃至褪去 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com