
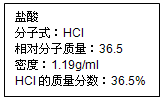
 如圖為實驗室某鹽酸試劑瓶標簽上的有關數據,試根據標簽上的有關數據回答下列問題:
如圖為實驗室某鹽酸試劑瓶標簽上的有關數據,試根據標簽上的有關數據回答下列問題:分析 (1)根據該物理量是否有溶液的體積有關判斷;
(2)依據容量瓶構造解答;
(3)依據配制溶液體積選擇合適規格容量瓶;依據C=$\frac{1000ρω}{M}$計算濃鹽酸的物質的量濃度,依據溶液稀釋過程中溶質的物質的量不變計算需要用鹽酸體積;
(4)分析操作對溶質的物質的量和溶液體積的影響,依據C=$\frac{n}{V}$進行誤差分析.
解答 解:(1)A.溶液中HCl的物質的量=nV,所以與溶液的體積有關,故A不選;
B.溶液具有均一性,濃度與體積無關,故B選;
C.溶液中Cl-的數目=nNA=CVNA,所以與溶液的體積有關,故c不選;
D.溶液的密度與溶液的體積無關,故D選;
故選:BD;
(2)容量瓶為配制一定物質的量濃度、一定體積溶液的專用儀器,標有:溫度、容積、刻度線,
故選:ACE;
(3)配制480mL物質的量濃度為0.400mol•L-1的稀鹽酸,應選擇500mL容量瓶,濃鹽酸的物質的量濃度C=$\frac{1000×1.19×36.5%}{36.5}$=11.9mol/L,設需要濃鹽酸體積為V,則依據溶液稀釋過程中溶質的物質的量不變得:11.9mol/L×V=0.4mol/L×500mL,解得V=16.8mL;
故答案為:A.16.8;
B.500mL容量瓶;
(4)①用量筒量取濃鹽酸時俯視觀察凹液面偏小,導致量取濃鹽酸體積偏小,溶質的物質的量偏小,溶液濃度偏小;
故答案為:偏小;
②溶液注入容量瓶前沒有冷卻至室溫,冷卻后溶液體積偏小,溶液濃度偏大;
故答案為:偏大.
點評 本題考查了配制一定物質的量濃度的溶液的方法,該題是中等難度的試題,試題基礎性強,貼近高考;該題難易適中,注重靈活性,側重對學生能力的培養和解題方法的指導和訓練,有利于培養學生的邏輯思維能力和嚴謹的規范實驗操作能力.


 王后雄學案教材完全解讀系列答案
王后雄學案教材完全解讀系列答案 海淀課時新作業金榜卷系列答案
海淀課時新作業金榜卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 取25 g CuSO4•5H2O溶于1 L水中 | |
| B. | 取16 g CuSO4•5H2O溶于少量水中,再稀釋至1 L | |
| C. | 取16 g無水CuSO4溶于1 L水中 | |
| D. | 取25 g CuSO4•5H2O溶于水配成1 L溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 反應:aA(g)+bB(g)?cC(g)△H<0 在2L恒容容器中進行.改變其他反應條件,在第一、第二和第三階段體系中各物質的物質的量隨時間變化的曲線如圖所示:
反應:aA(g)+bB(g)?cC(g)△H<0 在2L恒容容器中進行.改變其他反應條件,在第一、第二和第三階段體系中各物質的物質的量隨時間變化的曲線如圖所示:查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| 實驗順序 | 實驗內容 | 實驗現象 |
| ① | A+B | 無現象 |
| ② | B+D | 有氣體放出 |
| ③ | C+B | 有沉淀生成 |
| ④ | A+D | 有沉淀生成 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
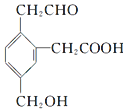 ,它在一定條件下可能發生的反應有( )
,它在一定條件下可能發生的反應有( )| A. | ②③④ | B. | ①③⑤⑥ | C. | ①③④⑤⑦ | D. | ②③④⑤⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溴水、FeCl3溶液 | B. | 溴水、酸性KMnO4溶液 | ||
| C. | 溴水、Na2CO3溶液 | D. | FeCl3溶液、酸性KMnO4溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CaCO3 | B. | NaOH | C. | H2SO4 | D. | CuO |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com