

分析 (1)Al3+水解生成的Al(OH)3膠體,具有吸附性;
(2)NH4Al(SO4)2水解,溶液呈酸性,升高溫度其水解程度增大;
(3)①a、b、c、d四個點,根據反應量的關系,a點恰好消耗完H+,溶液中只有(NH4)2SO4與Na2SO4;
②b點溶液呈中性,即溶液含有(NH4)2SO4、Na2SO4、NH3•H2O三種成分,所以b點時c(Na+)>c(SO42-),根據N元素與S元素的關系,可以得出c(SO42-)>c(NH4+),據此分析.
解答 解:(1)Al3+水解生成的Al(OH)3膠體,具有吸附性,離子方程式:Al3++3H2O?Al(OH)3膠體+3H+,
故答案為:Al3+水解生成的Al(OH)3膠體,具有吸附性,即Al3++3H2O?Al(OH)3膠體+3H+,Al(OH)3吸附懸浮顆粒使其沉降從而凈化水;
(2)NH4Al(SO4)2水解,溶液呈酸性,升高溫度其水解程度增大,pH減小,符合的曲線為Ⅰ,
故答案為:Ⅰ;NH4Al(SO4)2水解,溶液呈酸性,升高溫度,其水解程度增大,pH減小;
(3)①a、b、c、d四個點,根據反應量的關系,a點恰好消耗完H+,溶液中只有(NH4)2SO4與Na2SO4,b、c、d三點溶液均含有NH3•H2O,(NH4)2SO4可以促進水的電離,而NH3•H2O抑制水的電離,所以a水的電離程度最大,則在a點,反應的離子方程式為Al3++3OH-=Al(OH)3↓,故答案為:a;Al3++3OH-=Al(OH)3↓;
②b點溶液呈中性,即溶液含有(NH4)2SO4、Na2SO4、NH3•H2O三種成分,所以Al3+已經完全沉淀,故A正確,C錯誤;
b點溶液呈中性,b點時c(Na+)>c(SO42-),根據N元素與S元素的關系,可以得出c(SO42-)>c(NH4+),故c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+),故B正確;
又b點溶液呈中性,即溶液含有(NH4)2SO4、Na2SO4、NH3•H2O三種成分,則氫氧化鈉不僅使鋁離子沉淀還與部分銨根生成了氨水,所以消耗的NaOH溶液體積大于$\frac{0.1×0.1×3}{0.1}$L=300mL,故D正確;
故選:ABD.
點評 本題考查鹽類的水解和離子濃度大小的比較,題目難度較大,(3)②為易錯點,注意根據守恒思想解題.


科目:高中化學 來源: 題型:選擇題
| A. | O2 | B. | Cl2 | C. | HCl | D. | H2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 弱酸化學式 | CH3COOH | HCN | H2CO3 |
| 電離平衡常數(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | 1 mol•L-1的溶液中,pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) | |
| B. | 升高溫度,HCN溶液中H+濃度增大,平衡正向移動,電離平衡常數增大 | |
| C. | 向稀醋酸中逐滴加水,或加入少量冰醋酸,CH3COOH的電離平衡都正向移動 | |
| D. | 向CH3COOH溶液中加入少量氫氧化鈉固體,平衡正向移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
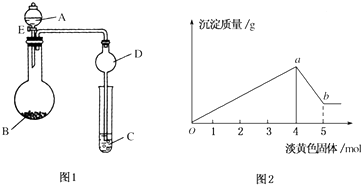
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 實驗方案(不要求寫出具體操作過程) | 預期實驗現象和結論 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 實驗室制NH3:NH4++OH-$\frac{\underline{\;△\;}}{\;}$NH3↑+H2O | |
| B. | NaOH與NH4Cl溶液混合加熱:NH4++OH-$\frac{\underline{\;△\;}}{\;}$NH3•H2O | |
| C. | 氨水中加鹽酸:NH3•H2O+H+═NH4++H2O | |
| D. | 氨氣通入稀H2SO4中:NH3+H+═NH4+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入無水CuSO4,再過濾 | |
| B. | 加入生石灰,再蒸餾 | |
| C. | 加入濃H2SO4,再加熱,蒸出乙醇 | |
| D. | 將96%的乙醇溶液直接加熱蒸餾出來 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 酸式鹽的水溶液一定顯堿性 | |
| B. | 只要酸和堿的物質的量濃度和體積分別相等,它們反應后的溶液就呈中性 | |
| C. | 純水呈中性是因為水中氫離子的物質的量濃度和氫氧根離子的物質的量濃度相等 | |
| D. | 碳酸溶液中氫離子的物質的量濃度是碳酸根離子的物質的量濃度的2倍 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com