
釩(V)及其化合物在工業催化、新材料和新能源等領域中有廣泛的應用,其中接觸法制硫酸工業中就要用到V2O5作催化劑:
2SO2(g)+O2(g)  2SO3(g) ΔH<0。
2SO3(g) ΔH<0。
某溫度下,將2 mol SO2和1 mol O2置于10 L密閉容器中,在V2O5作催化劑下經5min反應達平衡,SO2的平衡轉化率(α)為80%。
(1)5min內 v(SO3 )= mol·L-1·min-1
(2)該溫度下平衡常數K=
(3)若縮小容器體積,至達到新的平衡,在圖中畫出反應速率變化圖象。

(4)硫酸工業尾氣SO2用濃氨水吸收,反應的離子方程式是 ,吸收后的產物最終可制成肥料硫銨[即(NH4)2SO4]。
(5)某含釩化合物及硫酸的電池是利用不同價態離子對的氧化還原反應來實現化學能和電能相互轉化的裝置,其原理如下圖所示。

①用該電池電解(NH4)2SO4溶液生產(NH4)2S2O8(過二硫酸銨)。電解時均用惰性電極,陽極電極反應式可表示為 ;若電解得1mol(NH4)2S2O8,則電池左槽中H+將 (填“增大”或“減少”) mol。
②電池使用一段時間后對其進行充電,充電過程中,陽電極反應式為: 。
科目:高中化學 來源: 題型:
| 3 |
| 2 |
| 3 |
| 2 |

查看答案和解析>>
科目:高中化學 來源:湖北省“9+4”聯合體2010-2011學年高二下學期期中聯考化學試題 題型:022
釩(V)及其化合物廣泛應用于工業催化、新材料和新能源等領域.
(1)全釩液流儲能電池是利用不同價態離子對的氧化還原反應來實現化學能和電能相互轉化的裝置,其原理如圖所示.

①若左槽溶液顏色逐漸由藍變黃,其電極反應式為________________.
②放電過程中,右槽溶液顏色逐漸由________色變為________色.
③放電過程中氫離子的作用是:通過交換膜定向移動使電流通過溶液形成閉合回路和________;
④若充電時,左槽溶液中n(H+)的變化量為2 mol,則反應轉移的電子數為________.
(2)將CH4設計成燃料電池,其利用率更高,裝置如圖所示(A、B為多孔碳棒).持續通入甲烷,在標準狀況下,消耗甲烷的體積為V L.

①0<V≤44.8 L時,電池總反應方程式為________________;
②44.8 L<V≤89.6 L時,負極電極反應為________________;
③V=67.2 L時,溶液中離子濃度大小關系為________________.
查看答案和解析>>
科目:高中化學 來源: 題型:
釩(V)及其化合物在工業催化、新材料和新能源等領域中有廣泛的應用,其中接觸法制硫酸工業中就要用到V2O5作催化劑:
2SO2(g)+O2(g) 2SO3(g) ΔH<0。
某溫度下,將2mol SO2和1mol O2置于10 L密閉容器中,在V2O5作催化劑下經5min反應達平衡,SO2的平衡轉化率(α)為80%。
(1)5min內 v(SO3 )= mol·L-1·min-1
(2)該溫度下平衡常數K=
(3)若縮小容器體積,至達到新的平衡,在圖中畫出反應速率變化圖象。
(4)硫酸工業尾氣SO2用濃氨水吸收,反應的離子方程式是 ,吸收后的產物最終可制成肥料硫銨[即(NH4)2SO4]。
(5)某含釩化合物及硫酸的電池是利用不同價態離子對的氧化還原反應來實現化學能和電能相互轉化的裝置,其原理如下圖所示。
①用該電池電解(NH4)2SO4溶液生產(NH4)2S2O8(過二硫酸銨)。電解時均用惰性電極,陽極電極反應式可表示為 ;若電解得1mol(NH4)2S2O8,則電池左槽中H+將 (填“增大”或“減少”) mol。
②電池使用一段時間后對其進行充電,充電過程中,陽電極反應式為: 。
查看答案和解析>>
科目:高中化學 來源:2012屆浙江省衢州二中高三下學期第一次綜合練習理科綜合試卷(化學部分) 題型:填空題
釩(V)及其化合物在工業催化、新材料和新能源等領域中有廣泛的應用,其中接觸法制硫酸工業中就要用到V2O5作催化劑:
2SO2(g)+O2(g)  2SO3(g) ΔH<0。
2SO3(g) ΔH<0。
某溫度下,將2 mol SO2和1 mol O2置于10 L密閉容器中,在V2O5作催化劑下經5min反應達平衡,SO2的平衡轉化率(α)為80%。
(1)5min內 v(SO3 )= mol·L-1·min-1
(2)該溫度下平衡常數K=
(3)若縮小容器體積,至達到新的平衡,在圖中畫出反應速率變化圖象。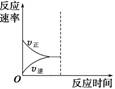
(4)硫酸工業尾氣SO2用濃氨水吸收,反應的離子方程式是 ,吸收后的產物最終可制成肥料硫銨[即(NH4)2SO4]。
(5)某含釩化合物及硫酸的電池是利用不同價態離子對的氧化還原反應來實現化學能和電能相互轉化的裝置,其原理如下圖所示。
①用該電池電解(NH4)2SO4溶液生產(NH4)2S2O8(過二硫酸銨)。電解時均用惰性電極,陽極電極反應式可表示為 ;若電解得1mol(NH4)2S2O8,則電池左槽中H+將 (填“增大”或“減少”) mol。
②電池使用一段時間后對其進行充電,充電過程中,陽電極反應式為: 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com