
分析 (1)化學平衡常數,是指在一定溫度下,可逆反應達到平衡時各生成物濃度的化學計量數次冪的乘積除以各反應物濃度的化學計量數次冪的乘積所得的比值,據此書寫,注意固體、醇液體不需要寫出;
根據v=$\frac{△c}{△t}$計算v(NO),再 利用速率之比等于化學計量數之比計算v(N2);
(2)提高NO的轉化率,改變條件使平衡向正反應移動,注意不能增大NO的濃度;
(3)若開始時密閉容器的體積為1L,其它條件不變,等效為增大壓強,該反應前后氣體的物質的量不變,平衡不移動,與原平衡為等效平衡,據此結合選項判斷.
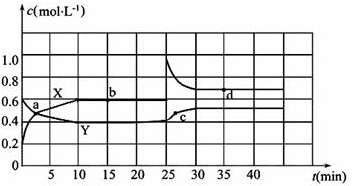
解答 解:(1)可逆反應C(s)+2NO(g)?N2(g)+CO2(g)平衡常數k=$\frac{{[{N_2}]•[CO]}}{{{{[NO]}^2}}}$.30min后達到平衡,測得NO濃度為0.04mol/L,則△c(NO)=$\frac{0.2mol}{2L}$=0.1mol/L-0.04mol/L=0.06mol/L,故v(NO)=$\frac{0.06mol/L}{30min}$=0.002mol/(L•min),速率之比等于化學計量數之比,故v(N2)=$\frac{1}{2}$v(NO)=$\frac{1}{2}$×0.002mol/(L•min)=0.001 mol/(L•min),
故答案為:$\frac{{[{N_2}]•[CO]}}{{{{[NO]}^2}}}$;0.001 mol/(L•min);
(2)該反應正反應是放熱反應,降低溫度可以使平衡向正反應移動,提高NO的轉化率,除去二氧化碳以使平衡向正反應移動,提高NO的轉化率,
故答案為:降溫、除去二氧化碳;
(3)若開始時密閉容器的體積為1L,其它條件不變,等效為增大壓強,該反應前后氣體的物質的量不變,平衡不移動,與原平衡為等效平衡,
a.平衡不移動,與原平衡為等效平衡,NO的轉化率不變,故a正確;
b.平衡時N2的物質的量不變,體積縮小一倍,故濃度是原來的2倍,故b正確;
c.NO的轉化率不變,參加反應的NO的物質的量與原平衡相同為0.2mol-0.04mol/L×2L=0.12mol,故反應放出的熱量為$\frac{0.12mol}{2mol}$×Q=0.06Q,故c錯誤;
d.壓強增大一倍,反應速率加快,但不一定是原平衡的2倍,故達到平衡的時間不一定原來的一半,故d錯誤;
故答案為:ab.
點評 本題考查化學平衡問題,為高頻考點,側重于學生的分析能力和計算能力的考查,題目涉及化學平衡常數、反應速率計算、化學平衡計算與影響因素等,難度中等,(3)中注意理解等效平衡規(guī)律.


科目:高中化學 來源: 題型:解答題
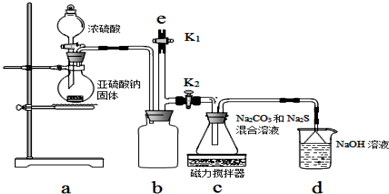
 為了分別研究SO2和Cl2的性質,設計了如圖1所示的實驗裝置.
為了分別研究SO2和Cl2的性質,設計了如圖1所示的實驗裝置.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

| 物質 | 沸點/℃ | 熔點/℃ | 密度(20℃)/(g/cm3) | 溶解性 |
| 甲醇 | 64.7 | - | 0.795 | 易溶于水 |
| 乙醚 | 34.5 | - | 0.7138 | 難溶于水 |
| 3,5-二甲氧基苯酚 | 172 | 36 | - | 易溶于甲醇、乙醚、微溶于水 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
 某課外活動小組探索苯與液溴的反應是否屬于取代反應,設計了如下實驗裝置.
某課外活動小組探索苯與液溴的反應是否屬于取代反應,設計了如下實驗裝置.
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 制乙烯時,用排水法或向上排空氣法收集氣體 | |
| B. | 制氯氣時,用飽和NaHCO3溶液和濃硫酸凈化氣體 | |
| C. | 制氧氣時,用Na2O2或H2O2作反應物可選擇相同的氣體發(fā)生裝置 | |
| D. | 制二氧化氮時,用水或NaOH溶液吸收尾氣 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com