
【題目】I.常溫常壓下,一氧化二氯(Cl2O)為棕黃色氣體。沸點為3.8℃,當溫度高于42℃時,分解生成Cl2和O2,Cl2O易溶于水并與水反應生成HClO。將氯氣和空氣(不參與反應)按照體積比1:3混合后,通入含水量為8%(質量分數)的碳酸鈉中制備Cl2O,并用水吸收Cl2O(不含Cl2)制備次氯酸溶液。

(1)儀器a的名稱是 ________________。
(2)上述裝置合理的連接順序為 ___ →___ →___ → C →___ →(填裝置下方的大寫字母)。
(3)反應過程中裝置B需要放在冷水中,其目的是________________________________。
(4)裝置C的作用 __________________________________。
(5)制備Cl2O的化學方程式____________________________________________。
(6)此方法相對于用氯氣直接溶于水制備次氯酸溶液的優點主要為_________________。
II.(7)探究NO與Na2O2反應的產物。
假設1:產物只有NaNO2;
假設2:__________;
假設3:產物為NaNO3和NaNO2的混合物。
為驗證反應產物,該小組同學準確稱取反應后的固體3.50 g,用煮沸并冷卻后的蒸餾水配成100.00 mL溶液,取10.00 mL溶液于錐形瓶中,用0.200 0 mol·L-1KMnO4溶液(硫酸酸化)滴定,共消耗KMnO4溶液10 mL。滴定過程中發生反應的離子方程式為_______________,反應產物中NaNO2的質量分數為_________(保留四位有效數字)。
【答案】三頸燒瓶 A D B E 防止反應放熱后溫度過高導致Cl2O分解 除去Cl2O中的Cl2 2Cl2 + Na2CO3=Cl2O + 2NaCl + CO2或2Cl2 + Na2CO3 + H2O =Cl2O + 2NaCl +H2 CO3或2Cl2 + Na2CO3 + H2O =Cl2O + 2NaCl +NaHCO3 制得的次氯酸溶液純度較高(濃度較大) 產物只有NaNO3 2MnO4—+5NO2—+6H+=5NO3—![]() +2Mn2++3H2O 98.57%
+2Mn2++3H2O 98.57%
【解析】
I.根據實驗目的,要將Cl2和空氣混合通入含Na2CO3溶液中制備Cl2O ,應先用裝置A制備Cl2,再通過裝置D除去混合氣體中的HCl氣體,同時混入空氣,將混合氣體通入裝置B,在裝置B中發生制備Cl2O 的反應;然后將制取的Cl2O氣體先通入裝置C,以除去Cl2雜質氣體,最后通過裝置E制取次氯酸溶液。
II.由化合價變化可知,NO與Na2O2反應可能生成NaNO2或NaNO3或NaNO3和NaNO2的混合物;NaNO2中N元素為+3價,能被酸性KMnO4溶液氧化為NaNO3,根據方程式和題給數據計算反應產物中NaNO2的質量分數。
I.(1)儀器a的名稱是三頸燒瓶,故答案為:三頸燒瓶;
(2)根據實驗目的,要將Cl2和空氣混合通入含Na2CO3溶液中制備Cl2O ,應先用裝置A制備Cl2,再通過裝置D除去混合氣體中的HCl氣體,同時混入空氣,將混合氣體通入裝置B,在裝置B中發生制備Cl2O 的反應;然后將制取的Cl2O氣體先通入裝置C,以除去Cl2雜質氣體,最后通過裝置E制取次氯酸溶液,故裝置的連接順序為A、D、B、C、E,故答案為:A;D;B;E;
(3)已知Cl2O 在42℃以上會分解生成Cl2和O2,因此反應過程中,裝置B需放在冷水中,防止反應放熱后溫度過高導致Cl2O分解,故答案為:防止反應放熱后溫度過高導致 Cl2O 分解;
(4)氯氣屬于非極性分子,易溶于非極性的有機溶劑四氯化碳,所以裝置 C 的作用是除去 Cl2O 中的Cl2,故答案為:除去 Cl2O 中的 Cl2;
(5)氯氣與碳酸鈉溶液發生歧化反應,其中氯元素從0價變為+1價和-1價,生成Cl2O和NaCl,反應的方程式為:2Cl2+Na2CO3=Cl2O+2NaCl+CO2(或 2Cl2+2Na2CO3+H2O=Cl2O+2NaCl+2NaHCO3),故答案為:2Cl2+Na2CO3=Cl2O+2NaCl+CO2(或 2Cl2+2Na2CO3+H2O=Cl2O+2NaCl+2NaHCO3);
(6)氯氣直接溶于水反應生成鹽酸和次氯酸的反應為可逆反應,制備的次氯酸濃度較低,并且有鹽酸雜質,而用此方法制備次氯酸溶液純度較高、濃度較大,故答案為:制得的次氯酸溶液純度較高(濃度較大);
II.(7)由化合價變化可知,NO與Na2O2反應可能生成NaNO2或NaNO3或NaNO3和NaNO2的混合物,故答案為:NaNO3;
NaNO2中N元素為+3價,能被酸性KMnO4溶液氧化為NaNO3,離子反應為2MnO4-+5NO2-+6H+
=5NO3-+2Mn2++3H2O,滴定過程中消耗KMnO4的物質的量是2×10-3mol,根據方程式可知參加反應的NaNO2的物質的量為5×10-3mol,質量為5×10-3mol×69g/mol=0.345g,被滴定的10mL溶液中含有0.35g反應后的固體,則反應產物中NaNO2的質量分數為0.345g÷0.35g
×100%=98.57%,故答案為:2MnO4-+5NO2-+6H+=5NO3-+2Mn2++3H2O;98.57%。


科目:高中化學 來源: 題型:
【題目】1 mol H—H鍵的鍵能是436kJ,1 mol I—I鍵的鍵能是151kJ,1 mol H—I鍵的鍵能是299kJ,則對反應H2(g)+I2(g)![]() 2HI(g)的說法,不正確的是 ( )
2HI(g)的說法,不正確的是 ( )
A.放熱反應B.吸熱反應C.化合反應D.可逆反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】固態或氣態碘分別與氫氣反應的熱化學方程式如下:
①H2(g)+I2(?)2HI(g)△H=-9.48kJmol-1
②H2(g)+I2(?)2HI(g)△H=+26.48kJmol-1
下列判斷不正確的是( )
A.![]() 中的I2為氣態,
中的I2為氣態,![]() 中的I2為固態
中的I2為固態
B.![]() 的反應物總能量比
的反應物總能量比![]() 的反應總能量低
的反應總能量低
C.1mol固態碘升華時將吸熱35.96kJ
D.反應![]() 的產物比反應
的產物比反應![]() 的產物熱穩定性更好
的產物熱穩定性更好
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在某無色酸性溶液中能大量共存的一組離子是
A.Na+、K+、HCO3、NO3 B.NH4+、SO42、Al3+、NO3
C.Na+、Ca2+、NO3、CO32 D.K+、MnO4、NH4+、NO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值。下列有關敘述正確的是
A. 標準狀況下,22.4LCHCl3中含有的分子數為NA
B. 1L 0.1mol·L-1的NaHS溶液中HS-和S2-離子數之和為0.1NA
C. 白磷結構如圖所示,12.4g白磷中所包含的P—P共價鍵有0.6NA

D. 在標準狀況下,含4molHCl的濃鹽酸與足量的MnO2反應可生成22.4L氯氣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I.NO是第一個被發現的生命體系氣體信號分子,具有舒張血管的功能。工業上可用“氨催化氧化法”生產NO,主要副產物為N2。請回答下列問題:
(1)以氨氣、氧氣為原料,在催化劑存在下生成NO和副產物N2的熱化學方程式如下:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H1①,4NH3(g)+3O2(g)
4NO(g)+6H2O(g) △H1①,4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g) △H2②,N2(g)+O2(g)
2N2(g)+6H2O(g) △H2②,N2(g)+O2(g)![]() 2NO(g) △H3③,則上述反應熱效應之間的關系式為△H3 =___________________。
2NO(g) △H3③,則上述反應熱效應之間的關系式為△H3 =___________________。
(2)某化學研究性學習小組模擬工業合成NO的反應。在1110K時,向一恒容密閉容器內充入1mol NH3和2.8mol O2,加入合適催化劑(催化劑的體積大小可忽略不計),保持溫度不變,只發生反應4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H<0。
4NO(g)+6H2O(g) △H<0。
①下列各項能說明反應已達到化學平衡狀態的是_______。(填字母序號)
a.5c(NH3)=4c(O2)
b.N-H鍵的生成速率與O-H鍵的生成速率相等
c.混合氣體的壓強不變
d.混合氣體的密度不變
②若其他條件不變,將容器改為恒容的絕熱容器,在達到平衡后的體系溫度下的化學平衡常數為K1,則K1_____K(填“>”、“<”或“=”)。
II.(3)某化學研究性學習小組模擬用CO和H2合成甲醇,其反應為:CO(g)+2H2(g) ![]() CH3OH(g)△H<O。在容積固定為1L的密閉容器內充入2mol CO和4 mol H2,加入合適的催化劑(體積可以忽略不計)、保持250℃不變發生上述反應,用壓力計監測容器內壓強的變化如下:
CH3OH(g)△H<O。在容積固定為1L的密閉容器內充入2mol CO和4 mol H2,加入合適的催化劑(體積可以忽略不計)、保持250℃不變發生上述反應,用壓力計監測容器內壓強的變化如下:
反應時間/min | 0 | 5 | 10 | 15 | 20 | 25 |
壓強/MPa | 12.4 | 10.2 | 8.4 | 7.0 | 6.2 | 6.2 |
則反應從開始到20min時,以CO濃度變化表示的平均反應速率v(CO)=_______,該溫度下平衡常數K=_______。
III.(4)以甲烷為燃料的新型電池,其成本大大低于以氫氣為燃料的傳統燃料電池,目前得到廣泛的研究,下圖是目前研究較多的一類固體氧化物燃料電池工作原理示意圖。回答下列問題:

①B極上的電極反應式為_____________。
②若用該燃料電池作電源,用石墨作電極電解硫酸銅溶液,當陽極收集到5.6 L(標準狀況)氣體時,消耗甲烷的體積為________L(標準狀況下)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組探究SO2與FeCl3溶液的反應,所用裝置如圖所示(夾持儀器已略去)。
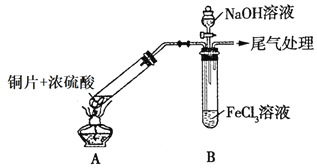
(1)圖中盛放NaOH溶液的玻璃儀器名稱是______。
(2)實驗前,應先檢查裝置的______;實驗開始后,A裝置中試管內發生反應的化學方程式為______。實驗中產生尾氣可通入______(填寫化學試劑)進行吸收處理。
(3)B試管中裝有5mL1molL-1FeCl3溶液,往其中通入足量的SO2氣體,B試管中的實驗現象為______,寫出該反應的離子方程式______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質的分類合理的是( )
A. 非電解質:氨氣、酒精、氯氣
B. 混合物:鹽酸、堿石灰、純牛奶
C. 堿:燒堿、純堿、氫氧化鋇
D. 酸性氧化物:CO2、SiO2、Na2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學生探究0.25 mol·L-1 Al2(SO4)3溶液與0.5 mol·L-1 Na2CO3溶液的反應,實驗如下。下列分析錯誤的是
實驗1 |
|
實驗2 |
|
A. 實驗1中,白色沉淀a是Al(OH)3
B. 實驗2中,白色沉淀b中含有CO![]()
C. 檢驗白色沉淀a、b是否洗滌干凈,不可使用相同的檢驗試劑
D. 實驗1、2中,白色沉淀成分不同可能與混合后溶液的pH有關
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com