
一定溫度下可逆反應:A(s)+2B(g) 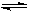 2C(g)+D(g);?H<0。現將1 mol A和2 mol B加入甲容器中,將4 mol C和2 mol D加入乙容器中,此時控制活塞P,使乙的容積為甲的2倍,t1時兩容器內均達到平衡狀態(如圖1所示,隔板K不能移動)。下列說法正確的是
2C(g)+D(g);?H<0。現將1 mol A和2 mol B加入甲容器中,將4 mol C和2 mol D加入乙容器中,此時控制活塞P,使乙的容積為甲的2倍,t1時兩容器內均達到平衡狀態(如圖1所示,隔板K不能移動)。下列說法正確的是

A.保持溫度和活塞位置不變,在甲中再加入1 mol A和2 mol B,達到新的平衡后,甲中C的濃度是乙中C的濃度的2倍
B.保持活塞位置不變,升高溫度,達到新的平衡后,甲、乙中B的體積分數均減少
C.保持溫度和乙中的壓強不變,t2時分別向甲、乙中加入等質量的氦氣后,甲、乙中反應速率變化情況分別如圖2和圖3所示(t1前的反應速率變化已省略)
D.保持溫度不變,移動活塞P,使乙的容積和甲相等,達到新的平衡后,乙中C的體積分數是甲中C 的體積分數的2倍
科目:高中化學 來源:2016屆江蘇省高三考前熱身(五模)化學試卷(解析版) 題型:選擇題
用下列裝置進行相應實驗,能達到實驗目的的是
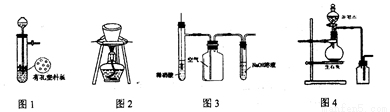
A. 圖1所示裝置用于Cu和濃硫酸反應制取少量的SO2氣體
B. 圖2裝置用于除去碳酸氫鈉固體中的少量碳酸鈉
C. 圖3裝置用于制備并收集NO氣體
D. 圖4所示裝置制取并收集氨氣
查看答案和解析>>
科目:高中化學 來源:2016屆安徽省高三下沖刺模擬理綜化學C卷(解析版) 題型:選擇題
設NA為阿伏加羅常數的值,下列說法正確的是( )
A.34g質量分數為4%的H2O2水溶液中含氧原子數目為0.08NA
B.反應3H2(g)+N2(g) 2NH3(g) △H=-92kJ/mol,若放出熱量4.6kJ,則轉移電子數目為0.3NA
2NH3(g) △H=-92kJ/mol,若放出熱量4.6kJ,則轉移電子數目為0.3NA
C.常溫常壓下,28g乙烯與丙烯的混合氣體中含有的碳原子數目無法計算
D.6.4gCu與40mL10mol•L-1濃硝酸作用能生成NO2的分子數為0.2NA
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧沈陽二中高一6月月考化學試卷(解析版) 題型:簡答題
煤化工中常需研究不同溫度下平衡常數、投料比及產率等問題。
已知CO(g)+H2O(g)  H2(g)+CO2(g)的平衡常數隨溫度的變化如下表:
H2(g)+CO2(g)的平衡常數隨溫度的變化如下表:

試回答下列問題:
(1)上述反應的正反應是________反應(填“放熱”或“吸熱”)。
(2)某溫度下,上述反應達到平衡后,保持容器體積不變升高溫度,逆反應速率________(填“增大”、“減小”或“不變”),容器內混合氣體的壓強________(填“增大”、“減 小”或“不變”)。
(3)830 ℃時,在恒容反應器中發生上述反應,按下表中的物質的量投入反應混合物,其中向逆反應方向進行的有______(選填字母)
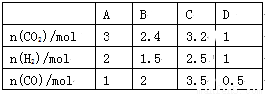
(4)在830 ℃時,在2 L的密閉容器中加入4 mol CO(g)和6 mol H2O(g)達到平衡時,H2(g)的體積分數是__________。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧沈陽二中高一6月月考化學試卷(解析版) 題型:選擇題
X、Y、Z、W、R屬于短周期主族元素。X的原子半徑是短周期主族元素中最大的,Y元素的原子最外層電子數為m,次外層電子數為n,Z元素的原子L層電子數為m+n,M層電子數為m—n,W元素與Z元素同主族,R元素原子與Y元素原子的核外電子數之比為2:1。 下列敘述錯誤的是
A. X與Y形成的兩種化合物中陰、陽離子的個數比均為1∶2
B. Y的氫化物比R的氫化物穩定,熔沸點高
C. Z、W、R最高價氧化物對應水化物的酸性強弱順序是:R>W>Z
D. RY2、WY2通入Ba(NO3)2溶液中均無白色沉淀生成。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧沈陽二中高一6月月考化學試卷(解析版) 題型:選擇題
將固體NH4I置于密閉容器中,在一定溫度下發生下列反應:①NH4I(s) NH3(g)+HI(g) ②2HI(g)
NH3(g)+HI(g) ②2HI(g) H2(g)+I2(g) 達到平衡時,c(H2)=1.0 mol·L-1,c(HI)=4mol·L-1,則此溫度下反應①的平衡常數為
H2(g)+I2(g) 達到平衡時,c(H2)=1.0 mol·L-1,c(HI)=4mol·L-1,則此溫度下反應①的平衡常數為
A.16 B.20 C.24 D.36
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧沈陽二中高一6月月考化學試卷(解析版) 題型:選擇題
下列說法正確的是
A.其它條件相同時,增大反應物濃度能使分子獲得能量,活化分子百分數提高,反應速率增大
B.判斷過程的自發性能確定過程能否發生和過程發生的速率
C.體系有自發地向混亂度增加(即熵增)的方向轉變的傾向,這是自然界的普遍規律
D.催化劑不影響反應 活化能,從而只影響反應速率,不影響化學平衡
活化能,從而只影響反應速率,不影響化學平衡
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧沈陽二中高二6月小班成果驗收化學卷(解析版) 題型:選擇題
新型納米材料MFe2Ox(3<X<4)中,M表示+2價的金屬元素,在反應中化合價不發生變化。常溫下,MFe2Ox能使工業廢氣中的SO2轉化為S,轉化過程表示如下:
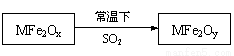
則下列判斷正確的是( )
A.MFe2Ox是還原劑 B.氧化性:MFe2Ox> SO2
C.X>Y D.SO2是該反應的催化劑
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江牡丹江一中高二6月月考化學試卷(解析版) 題型:選擇題
設NA表示阿伏加德羅常數的值,下列敘述中不正砷的是
A.1 mol Cl2與足量NaOH反應,轉移的電子數為NA
B.常溫常壓下,11.2 L甲烷中含有的氫原子數小于2 NA
C.1 mol碳烯(∶CH2 )所含的電子數目為6NA
D.T℃時,1 L pH=6的純水中含OH-數為10-6 NA
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com