
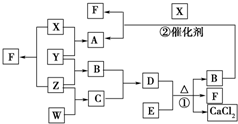
 X、Y、Z、W均為氣體單質,A、B、C均為無色氣體化合物,D、E均為白色固體,F在通常情況下為無色無味的液體,它們有如下的轉化關系:
X、Y、Z、W均為氣體單質,A、B、C均為無色氣體化合物,D、E均為白色固體,F在通常情況下為無色無味的液體,它們有如下的轉化關系: ,F中的化學鍵類型為共價鍵.
,F中的化學鍵類型為共價鍵.分析 X、Y、Z、W均為氣體單質,F在通常情況下為無色無味的液體,X與Z反應得到F,則F為H2O,X、Z分別為H2、O2中的一種,A、B、C均為無色氣體化合物,D、E均為白色固體,反應①是實驗式制備氨氣,則B為NH3,D、E分別為NH4Cl、Ca(OH)2中的一種,B與X反應得到A與F(水),則X為O2,A為NO,Z為H2,X與Y反應得到A,故Y為N2,B(氨氣)與C反應得到D,則D為NH4Cl、E為Ca(OH)2、C為HCl,而氣體單質W與Z反應得到C,故W為Cl2,據此解答.
解答 解:X、Y、Z、W均為氣體單質,F在通常情況下為無色無味的液體,X與Z反應得到F,則F為H2O,X、Z分別為H2、O2中的一種,A、B、C均為無色氣體化合物,D、E均為白色固體,反應①是實驗式制備氨氣,則B為NH3,D、E分別為NH4Cl、Ca(OH)2中的一種,B與X反應得到A與F(水),則X為O2,A為NO,Z為H2,X與Y反應得到A,故Y為N2,B(氨氣)與C反應得到D,則D為NH4Cl、E為Ca(OH)2、C為HCl,而氣體單質W與Z反應得到C,故W為Cl2.
(1)Y為N2,電子式為 ,F為H2O,含有的化學鍵類型為共價鍵,
,F為H2O,含有的化學鍵類型為共價鍵,
故答案為: ;共價鍵;
;共價鍵;
(2)C的化學式為HCl,故答案為:HCl;
(3)B在F中的反應可以表示為:NH3+H2O?NH3•H2O?NH4++OH-,
故答案為:NH3+H2O?NH3•H2O?NH4++OH-;
(4)反應①的化學方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,
故答案為:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
點評 本題考查無機物推斷,題目涉及物質比較多,熟練掌握氣體的實驗室制備與常見化學工業、元素化合物性質,題目難度中等.


科目:高中化學 來源: 題型:解答題
| 反應溫度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 產品回收率(%) | 75.6 | 78.4 | 80.6 | 82.6 | 83.1 | 82.1 | 73.7 |
| 反應物料比 | 2:1 | 3:1 | 4:1 | 5:1 | 6:1 | 7:1 |
| 產品回收率(%) | 0 | 38.4 | 82. 6 | 83.6 | 84.5 | 84.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
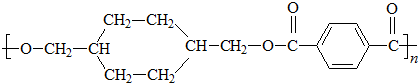
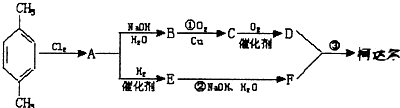
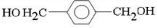 、D
、D 、E
、E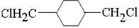 ;
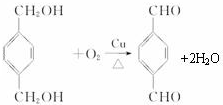
;
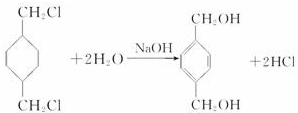 ;
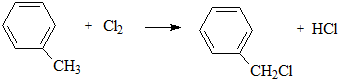
; +
+ $\stackrel{一定條件}{→}$
$\stackrel{一定條件}{→}$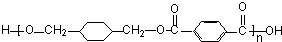 +(2n-1)H2O.
+(2n-1)H2O.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
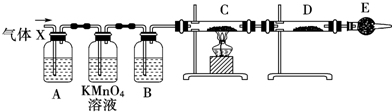
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH3、CO、CO2都是極性分子 | |
| B. | CH4、CCl4都是含有極性鍵的非極性分子 | |
| C. | HF、HCl、HBr、HI的穩定性依次增強 | |
| D. | CS2、H2O、C2H2都是直線形分子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
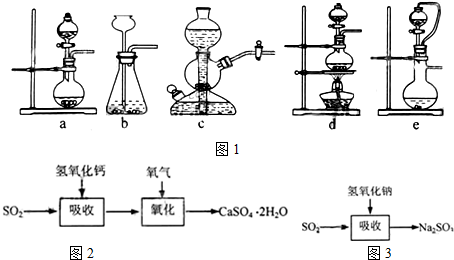
| 試劑 | Ca(OH)2 | NaOH |
| 價格(元/kg) | 0.36 | 2.9 |
| 吸收SO2的成本(元/mol) | 0.027 | 0.232 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 明礬凈水與液氯凈水的原理相同 | |
| B. | 將草木灰和硫銨混合施用,肥效更高 | |
| C. | 冬季形成的大霧屬于氣溶膠 | |
| D. | 電解精煉銅時,同一時間內陰極溶解銅的質量比陽極析出銅的質量小 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
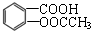 是一種常用的退熱、鎮痛藥物,臨床常用于預防心血管疾病.阿斯匹林對腸胃有一定的副作用,患有消化系統疾病的人不宜服用.則下列對此化合物說法不正確的是( )
是一種常用的退熱、鎮痛藥物,臨床常用于預防心血管疾病.阿斯匹林對腸胃有一定的副作用,患有消化系統疾病的人不宜服用.則下列對此化合物說法不正確的是( )| A. | 阿斯匹林能與NaHCO3反應,最多能與3mol H2發生加成反應 | |
| B. | 1 mol阿斯匹林與足量的NaOH溶液反應,消耗NaOH最大的物質的量為3 mol | |
| C. | 其苯環上的一氯取代物有兩種 | |
| D. | 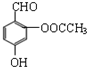 與阿斯匹林互為同分異構體,該有機物遇FeCl3溶液顯紫色 與阿斯匹林互為同分異構體,該有機物遇FeCl3溶液顯紫色 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com