
| A. | ②⑤⑥ | B. | ①②⑤ | C. | ③④⑥ | D. | ③④⑤ |
分析 ①溶解性大小與酸的電離的程度無關;
②酸與堿發生中和反應無法確定酸電離的程度;
③苯酚與氯化鐵溶液發生顯色反應;
④溴與苯酚發生取代反應,不能比較酸性強弱;
⑤苯酚不能使能紫色石蕊指示劑變紅;
⑥苯酚的酸性弱于碳酸,碳酸氫根離子的電離大于苯酚.
解答 解:①苯酚的渾濁液加熱后變澄清,說明溫度升高苯酚溶解度增大,無法說明苯酚的酸性,故①不選;
②苯酚的水溶液中加NaOH溶液,生成苯酚鈉,能說明苯酚溶液呈酸性,故②選;
③苯酚與氯化鐵溶液發生顯色反應,無法說明苯酚的酸性,故③不選;
④苯酚與氯化鐵溶液發生顯色反應,無法說明苯酚的酸性,故④不選;
⑤苯酚溶液中滴加紫色石蕊指示劑不變色,說明苯酚酸性弱,電離出的氫離子不足以使指示劑變色,故⑤選;
⑥苯酚能與Na2CO3溶液反應生成NaHCO3,說明苯酚酸性比弱酸碳酸弱,故⑥選;
故選A.
點評 本題考查了苯酚的性質,題目難度不大,注意苯酚和氯化鐵變色反應無法判斷酸性強弱、苯酚的酸性很弱,不能使指示劑變色.


 口算題卡北京婦女兒童出版社系列答案
口算題卡北京婦女兒童出版社系列答案科目:高中化學 來源: 題型:選擇題
 屠呦呦因對青蒿素的研究而獲得諾貝爾生理學或醫學獎,青蒿素可以青蒿酸(結構簡式如圖所示)為原料合成,下列關于青蒿酸的說法中正確的是( )
屠呦呦因對青蒿素的研究而獲得諾貝爾生理學或醫學獎,青蒿素可以青蒿酸(結構簡式如圖所示)為原料合成,下列關于青蒿酸的說法中正確的是( )| A. | 分子式為C15H24O2 | B. | 屬子芳香族化合物 | ||
| C. | 能發生取代反應和加成反應 | D. | 分子中所有原子可能共平面 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗編號 | 甲 | 乙 | 丙 |
| 樣品質量(g) | 9.6 | 12.8 | 64.0 |
| 氣體體積(L) | 5.04 | 6.72 | V |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
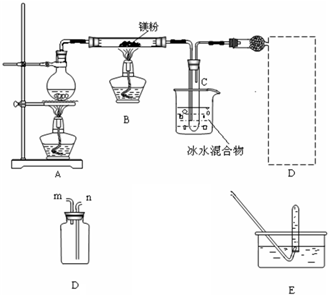
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | K=$\frac{[C]•[{H}_{2}O]}{[CO]•[{H}_{2}]}$ | B. | K=$\frac{[CO]•[{H}_{2}]}{[C]•[{H}_{2}O]}$ | C. | K=$\frac{[CO]•[{H}_{2}]}{[{H}_{2}O]}$ | D. | K=$\frac{[{H}_{2}O]}{[CO]•[{H}_{2}]}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
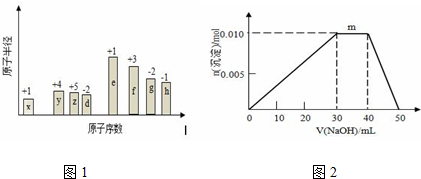
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Z元素的最高價氧化物對應的水化物酸性強于Y元素的最高價氧化物對應的水化物 | |
| B. | X、Y、Z形成的簡單離子的半徑大小:Yn->Zm->Xm- | |
| C. | 元素Z、Y分別與元素W形成的化合物的熱穩定性:WmZ<WnY | |
| D. | 若HnY溶液的酸性比HmZ溶液的酸性強,則Y的非金屬性比Z的強 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 元素 | 結構及性質 |
| A | A的原子半徑最小 |
| B | B原子最外層電子數是次外層的兩倍 |
| C | C元素在空氣中含量最多 |
| D | D是短周期中金屬性最強的元素 |
| E | E的最高價氧化物對應水化物是一種常見的兩性氫氧化物 |
| R | R與B同主族 |
| T | T的負一價陰離子的核外電子排布與Ar原子相同 |
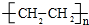 .
. ;它可用于潛艇或呼吸面具的供氧劑,它與H2O反應的化學方程式為2Na2O2+2H2O=4NaOH+O2↑.
;它可用于潛艇或呼吸面具的供氧劑,它與H2O反應的化學方程式為2Na2O2+2H2O=4NaOH+O2↑.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 實驗室用H2O2分解制O2,加入MnO2后,反應速率明顯加快 | |
| B. | 在金屬鈉與足量水反應中,增加水的量能加快反應速率 | |
| C. | 2SO2+O2?2SO3反應中,2molSO2在充足的氧氣中不能得到2molSO3 | |
| D. | 實驗室用碳酸鈣和鹽酸反應制取CO2,用碳酸鈣粉末比塊狀反應要快 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com