
(11分)Ⅰ:在H2O2作用下可實現Fe(CN)63-與Fe(CN)64-之間的相互轉化,在酸性溶液中H2O2可使Fe(CN)64-轉化為Fe(CN)63-;在堿性溶液里H2O2可使Fe(CN)63-轉化為Fe(CN)64-。寫出以上相互轉化的離子方程式。
① 酸性溶液中: ,
②堿性溶液中: 。
Ⅱ:膜技術原理在化工生產中有著廣泛的應用。有人設想利用電化學原理制備少量硫酸和綠色硝化劑N2O5,裝置圖如下。

(3)A裝置是________,B裝置是_________(填“原電池”或“電解池”)。
(4)N2O5在裝置中的______區(填“正、負極”或“陰、陽極”)生成,其電極反應式為______________。
(5)通入O2一極的電極反應式為_______________________________。
(1)2Fe(CN)64-+H2O2+2H+====2Fe(CN)63-+2H2O
(2) 2Fe(CN)63-+H2O2+2OH-====2Fe(CN)64-+2H2O+O2↑
(3)原電池 電解池
(4)陽極 N2O4+2HNO3-2e- 2N2O5+2H+
2N2O5+2H+
(5)O2+4H++4e- 2H2O
2H2O
【解析】
試題分析:1、過氧化氫具有氧化性在酸性條件下將Fe(CN)64-氧化成Fe (CN)63-
在堿性條件下,過氧化氫將氫氧根離子氧化成氧氣和水,Fe(CN)63-被還原為Fe(CN)64
3、根據兩個裝置圖可以看到B中兩個都是惰性電極,可知其是電解池。A為原電池。
4、氧氣通入的一級為正極,可以推出N2O4和無水硝酸在陽極 發生的電極方程式為 N2O4+2HNO3-2e- 2N2O5+2H+
2N2O5+2H+
5、氧氣在正極,得到電子被還原為水,O2+4H++4e- 2H2O
2H2O
考點:氧化還原反應,電解池和原電池,電極方程式的書寫
點評:本題屬于中等題,正確判斷出N2O4和無水硝酸在陽極反應時解題的關鍵。


 教學練新同步練習系列答案
教學練新同步練習系列答案科目:高中化學 來源: 題型:

| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
| 催化劑(0.1g) | 活性炭 | FeCl3 | KI | MnO2顆粒狀 | MnO2粉末狀 |
| 前15s產生氧氣的量(ml) | 5 | 11 | 7 | 8 | 11 |
| 前30s產生氧氣的量(ml) | 8 | 16 | 11 | 11 | 21 |
| 前45s產生氧氣的量(ml) | 11 | 20 | 15 | 18 | 35 |
| 前60s產生氧氣的量(ml) | 15 | 24 | 20 | 26 | 49 |
查看答案和解析>>
科目:高中化學 來源:2013屆湖南省師大附中高三第五次月考化學試卷(帶解析) 題型:填空題
(11分)Ⅰ:在H2O2作用下可實現Fe(CN)63-與Fe(CN)64-之間的相互轉化,在酸性溶液中H2O2可使Fe(CN)64-轉化為Fe(CN)63-;在堿性溶液里H2O2可使Fe(CN)63-轉化為Fe(CN)64-。寫出以上相互轉化的離子方程式。
① 酸性溶液中: ,
②堿性溶液中: 。
Ⅱ:膜技術原理在化工生產中有著廣泛的應用。有人設想利用電化學原理制備少量硫酸和綠色硝化劑N2O5,裝置圖如下。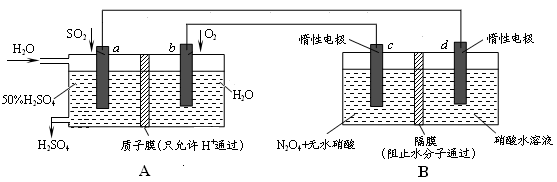
(3)A裝置是________,B裝置是_________(填“原電池”或“電解池”)。
(4)N2O5在裝置中的______區(填“正、負極”或“陰、陽極”)生成,其電極反應式為______________。
(5)通入O2一極的電極反應式為_______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
(14分)H2O2的水溶液是一種常用的殺菌劑,其質量百分比一般為3%和30%。
1-1 在H2O2作用下可實現Fe(CN)63-與Fe(CN)64-之間的相互轉化,在酸性溶液中H2O2可使Fe(CN)64-轉化為Fe(CN)63-;在堿性溶液里H2O2可使Fe(CN)63-轉化為Fe(CN)64-。寫出以上相互轉化的離子方程式 。
1-2 分別寫出實驗室、老工業、新工業制備H2O2的三種方法。
1-3 寫出二種定量測定H2O2水溶液中H2O2含量的化學方程式和簡要實驗步驟。
1-4 將H2O2溶液滴入含有酚酞的NaOH溶液中,紅色消失。甲學生認為這是由于H2O2是二元弱酸,消耗了OH-,而使紅色褪去;乙學生認為,H2O2具有強氧化性,將酚酞氧化,紅色消失。試設計一個實驗論證甲、乙兩位學生的解釋中哪種正確?
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com