
分析 (1)實驗時應先稱量一定質量的固體,溶解后配制成溶液,量取待測液與錐形瓶中,然后用標準液進行滴定;
(2)滴定管0刻度在上,滴定前應調節到零刻度或零稍下的某一刻度,為減小誤差,尖嘴部分應充滿液體,無氣泡;
(3)指示劑為甲基橙,變色范圍為3.1-4.4;
(4)根據反應消耗的硫酸,求出氫氧化鈉,進一步求出樣品的純度;
(5)①操作B中的堿式滴定管只用蒸餾水洗未用所盛燒堿溶液潤洗,堿溶液溶液被稀釋,則消耗的酸的體積偏小;
②酸式滴定管用蒸餾水洗滌后,直接裝入標準H2SO4溶液,酸被稀釋,酸的體積偏大;
③滴定時,錐形瓶搖動太劇烈,有少量液體濺出,堿溶液偏小,則消耗的酸的體積偏小;
④滴定到終點時,滴定管尖嘴部分懸有液滴,則讀出的酸的體積偏大;
⑤酸式滴定管讀數時滴定前仰視,滴定后俯視,讀出的酸的體積偏小.
解答 解:(1)實驗時應先稱量一定質量的固體,溶解后配制成溶液,量取待測液與錐形瓶中,然后用標準液進行滴定,
故答案為:C;A;B;E;
(2)將物質的量濃度為C mol/L的標準H2SO4溶液裝入酸式滴定管,調整液面到“0”刻度以下,故答案為:“0”刻度以下;
(3)硫酸滴定燒堿,甲基橙是指示劑,滴定至終點的現象是:當滴入最后一滴H2SO4溶液,錐形瓶內溶液由黃色變為橙色,并且半分鐘內不褪色.
故答案為:當滴入最后一滴H2SO4溶液,錐形瓶內溶液由黃色變為橙色,并且半分鐘內不褪色.
(4)滴到消耗的硫酸為:n(硫酸)=cV=(V2-V1)×10-3L×m mol/L,根據反應方程可知,n(NaOH)=2n(硫酸)=2m(V2-V1)×10-3mol,
所以原來樣品中氫氧化鈉的物質的量為:2m(V2-V1)×10-3mol×$\frac{250mL}{25}$=2m(V2-V1)×10-2mol,則樣品中氫氧化鈉的質量為m(NaOH)=nM=80m(V2-V1)×10-2g,則該燒堿樣品的純度為:$\frac{80c({V}_{2}-{V}_{1})×1{0}^{-2}g}{mg}$×100%=$\frac{0.8c({V}_{2}-{V}_{1})}{m}$×100%;
故答案為:$\frac{0.8c({V}_{2}-{V}_{1})}{m}$×100%;
(5)①操作B中的堿式滴定管只用蒸餾水洗未用所盛燒堿溶液潤洗,堿溶液溶液被稀釋,則消耗的酸的體積偏小,所以會導致測定結果偏低;
②酸式滴定管用蒸餾水洗滌后,直接裝入標準H2SO4溶液,酸被稀釋,酸的體積偏大,所以會導致測定結果偏高;
③滴定時,錐形瓶搖動太劇烈,有少量液體濺出,堿溶液偏小,則消耗的酸的體積偏小,所以會導致測定結果偏低;
④滴定到終點時,滴定管尖嘴部分懸有液滴,則讀出的酸的體積偏大,所以會導致測定結果偏高;
⑤酸式滴定管讀數時滴定前仰視,滴定后俯視,讀出的酸的體積偏小,所以會導致測定結果偏低;
故選②④.
點評 本題綜合考查酸堿中和滴定,側重于化學實驗基本操作以及物質的含量的測定等問題,題目難度中等,建議在學習中把握相關基本實驗方法,學習中注意積累.


 作業輔導系列答案
作業輔導系列答案 同步學典一課多練系列答案
同步學典一課多練系列答案 經典密卷系列答案
經典密卷系列答案科目:高中化學 來源: 題型:實驗題
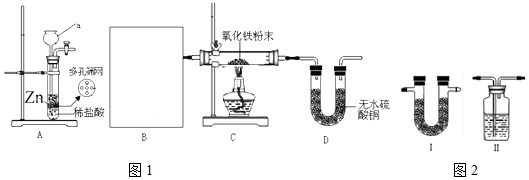
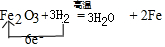 .實驗結束時應該采取的操作是先停止加熱,冷卻到室溫,再停止通H2.
.實驗結束時應該采取的操作是先停止加熱,冷卻到室溫,再停止通H2.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 無色透明的溶液中:Na+、SO42-、MnO4-、NO3- | |
| B. | 使無色酚酞試液呈紅色的溶液中:Na+、Cu2+、SO42-、Cl- | |
| C. | pH=1的溶液中:K+、ClO-、S2-、Cl- | |
| D. | 弱堿性的溶液中:Na+、K+、HCO3-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 滴定次數 | 待測NaOH溶液的體積/mL | 0.100 0mol•L-1鹽酸的體積/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液體積/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗次 序編號 | 鹽酸溶液體積 V/mL | 氫氧化鈉溶液體積 V/mL |
| 1 | 19.90 | 10.00 |
| 2 | 20.10 | 10.00 |
| 3 | 22.00 | 10.00 |
| 4 | 20.00 | 10.00 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 滴定次數 | 待測溶液 體積(mL) | 標準酸體積 | |
| 滴定前的刻度 (mL) | 滴定后的刻度 (mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
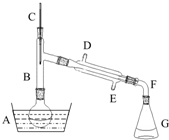 溴乙烷是一種重要的有機化工原料,制備溴乙烷的原料有95%乙醇、80%硫酸(用蒸餾水稀釋濃硫酸)、研細的溴化鈉粉末和幾粒碎瓷片,該反應的原理如下:NaBr+H2SO4=NaHSO4+HBr
溴乙烷是一種重要的有機化工原料,制備溴乙烷的原料有95%乙醇、80%硫酸(用蒸餾水稀釋濃硫酸)、研細的溴化鈉粉末和幾粒碎瓷片,該反應的原理如下:NaBr+H2SO4=NaHSO4+HBr| 物質 數據 | 乙醇 | 溴乙烷 | 1,2-二溴乙烷 | 乙醚 | 濃硫酸 |
| 密度/g•cm-3 | 0.79 | 1.46 | 2.2 | 0.71 | 1.84 |
| 熔點(℃) | -130 | -119 | 9 | -116 | 10 |
| 沸點(℃) | 78.5 | 38.4 | 132 | 34.6 | 338 |
| 在水中的溶解度(g) | 互溶 | 0.914 | 1 | 7.5 | 互溶 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
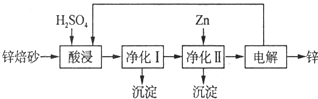
 ;
;
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com