
| ||
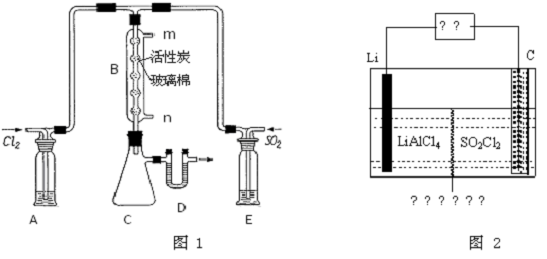
| c(SO2Cl2) |
| c(SO2)?c(Cl2) |
| c(SO2Cl2) |
| c(SO2)?c(Cl2) |
| ||
| ||


 期末寶典單元檢測分類復習卷系列答案
期末寶典單元檢測分類復習卷系列答案科目:高中化學 來源: 題型:
| HCl |
| 實驗 序號 | 初始濃度 c/mol?L-1 | 溴顏色消失 所需時間 t/s | ||
| CH3COCH3 | HCl | Br2 | ||
| ① | 0.8 | 0.2 | 0.001 | 290 |
| ② | 1.6 | 0.2 | 0.001 | 145 |
| ③ | 0.8 | 0.4 | 0.001 | 145 |
| ④ | 0.8 | 0.2 | 0.001 | 580 |
| A、v (Br2)與c(CH3COCH3)成正比 |
| B、增大c(Br2),v (Br2)變小 |
| C、增大c(HCl),v (Br2)增大 |
| D、實驗②和③的v (Br2)相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、氟化氫的電子式:H:F |
| B、乙醇的分子式:CH3CH2OH |
C、硫原子的結構示意圖: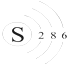 |
| D、Na2O2中即含有離子鍵,又含有非極性共價鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、CO2 |
| B、HCl(氣態) |
| C、Fe(OH)3膠體 |
| D、NaOH溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:
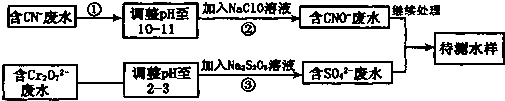
2- 7 |
2- 7 |
2- 7 |
查看答案和解析>>
科目:高中化學 來源: 題型:
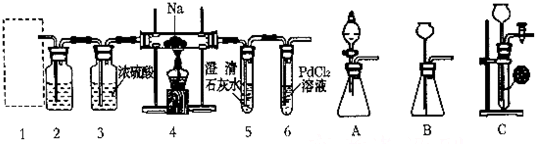
查看答案和解析>>
科目:高中化學 來源: 題型:
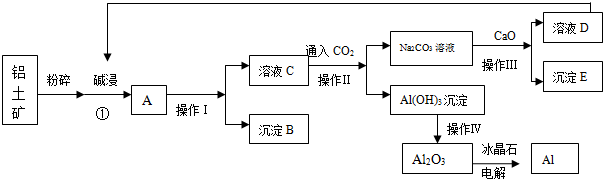
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com