


 七彩題卡口算應用一點通系列答案
七彩題卡口算應用一點通系列答案科目:高中化學 來源: 題型:
| A、32 g O2所含的原子數目為NA |
| B、1 mol氫約含有6.02×1023個微粒 |
| C、標準狀況下,2NA 個H2O的體積約為44.8 L |
| D、標準狀況下,22.4 L CH4和H2的混合氣體中含有NA個分子 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
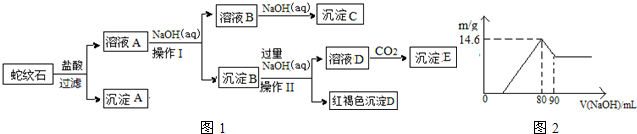
| 氫氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 開始沉淀pH | 1.9 | 3.3 | 9.4 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
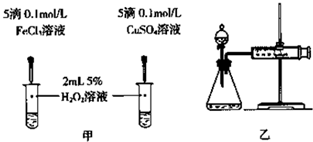
 某興趣小組設計研究銅和稀硝酸反應速率[v (NO)]的實驗.試回答下列問題:
某興趣小組設計研究銅和稀硝酸反應速率[v (NO)]的實驗.試回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com