
| 煅燒 |
| H2O |
| NaOH(aq) |
| 電解 |
| 稀H2SO4 |
| 在空氣中灼燒 |
| 蒸發 |
| 提取NaCl |
| Na2CO3溶液 |
| NaBr |
| NaBr |
| Cl2 |
| 熱空氣 |
| A、①③⑤ | B、②③④ |
| C、②④⑤ | D、①④⑤ |
| 煅燒 |
| NaOH(aq) |
| 少量HCl或通入CO2 |
| 稀H2SO4 |
| NaOH |
| 空氣中灼燒 |


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
| A、2.4g金屬鎂變成鎂離子時失去的電子數目為0.1NA |
| B、2g氫氣所含分子數目為2NA |
| C、在25C,1.01×1O5Pa時,11.2L氮氣所含的原子數目為NA |
| D、含3.01×1023個SO42-的Na2S04容液中,Na+數目為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:
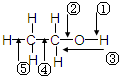 乙醇分子中各化學鍵如圖所示,對乙醇在各種反應中應斷裂的鍵說明正確的是( )
乙醇分子中各化學鍵如圖所示,對乙醇在各種反應中應斷裂的鍵說明正確的是( )| A、和金屬鈉作用時,鍵②斷裂 |
| B、和濃硫酸共熱至170℃時,②鍵和⑤斷裂 |
| C、在銅催化下和氧氣反應時,鍵①和③斷裂 |
| D、與氫鹵酸反應時,鍵①斷裂 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、0.43g |
| B、0.87g |
| C、13.1g |
| D、16.2g |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、Na、K、Cl、S |
| B、F、I、Fe、Zn、 |
| C、N、H、O、P |
| D、Ge、Se、Cu、Al、 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、2.24L |
| B、4.48L |
| C、6.72L |
| D、8.96L |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、N2的摩爾質量是14g |
| B、1mol H2O的質量是18g |
| C、氫氣的摩爾質量是1g?mol |
| D、1mol H2O 中含有1molH2和1mol0 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、一定量的Fe與含1mol HNO3的稀硝酸恰好反應,則被還原的氮原子數小于NA |
| B、1L 0.5mol/L Na2CO3溶液中含有的CO32-數目為0.5NA |
| C、標準狀況下,2.24L Cl2與足量的Mg充分反應,轉移的電子數目為0.2NA |
| D、0.1mol CH4所含的電子數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com