
分析 (1)電解質溶液:①Na2CO3 溶液中碳酸根離子水解顯堿性,②NaHCO3 溶液中碳酸氫根離子水解顯堿性,③CH3COONa 醋酸根離子水解顯堿性,④NaOH氫氧化鈉是強堿溶液;依據陰離子水解程度分析判斷;
(2)四種溶液濃度相同,稀釋相同倍數,稀釋促進鹽類水解,根據是否存在平衡分析判斷,不存在平衡的pH值變化大.
解答 解:(1)氫氧化鈉是強堿,不水解,相同濃度的三種溶液氫氧化鈉的pH最大,所以pH相同的三種溶液中,氫氧化鈉濃度最低,已知酸性:CH3COOH>H2CO3>HCO3->CO32-,所以碳酸鈉的水解程度大于碳酸氫鈉,大于醋酸鈉,則當四種溶液的pH相同時,其物質的量濃度由大到小的順序是③②①④,
故答案為:③②①④;
(2))①②③都存在水解平衡,當稀釋時,鹽的弱酸根又水解出部分離子進行補充;氫氧化鈉是強堿,完全電離,不存在電離平衡,所以當稀釋時,其pH變化最大,
故答案為:④.
點評 本題考查了溶液酸堿性與溶液pH的關系、弱電解質的電離、鹽的水解原理及其影響等知識,題目難度中等,明確鹽的水解原理、弱電解質的電離平衡及其影響因素為解答關鍵,注意掌握溶液酸堿性與溶液pH的關系.


科目:高中化學 來源: 題型:選擇題
| A. | 向Ca(ClO)2中通入少量SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| B. | 醋酸與水垢中的CaCO3反應:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 向AlCl3溶液中加入過量的氨水:Al3++4NH3•H2O═AlO2-+4NH4+ | |
| D. | NO2與水的反應:3NO2+H2O═2NO3-+NO+2H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | v(Fe)=0.5mol•(L•min)-1 | B. | v(H2SO4)=1mol•(L•min)-1 | ||
| C. | v(H2)=0.5mol•(L•min)-1 | D. | v=(FeSO4)=0.5mol•(L•min)-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 酸式滴定管滴至終點對,俯視讀數 | |
| B. | 錐形瓶用蒸餾水洗后,未干燥 | |
| C. | 酸式滴定管用蒸餾水洗后,未用標準液潤洗 | |
| D. | 酸式滴定管滴定至終點后,發現尖嘴處有氣泡(原來無氣泡) |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
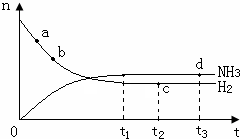 氨氣是一種重要的化工原料,大量用于制造尿素、純堿、銨態氮肥以及硝酸,在有機合成工業中制合成纖維、塑料、染料等.請回答下列問題:
氨氣是一種重要的化工原料,大量用于制造尿素、純堿、銨態氮肥以及硝酸,在有機合成工業中制合成纖維、塑料、染料等.請回答下列問題:| 容器編號 | 起始時各物質物質的量/mol | 平衡時反應 | ||
| N2 | H2 | NH3 | ||
| a | 1 | 3 | 0 | 23.1 |
| b | 2 | 6 | 0 | 未知(用E表示) |
| 容器 | c(CO2) /mol•L-1 | c(H2) /mol•L-1 | c(CH3OCH3) /mol•L-1 | c(H2O) /mol•L-1 | v (正)和v (逆)比較 |
| 容器I | 1.0×10-2 | 1.0×10-2 | 1.0×10-4 | 1.0×10-4 | v (正)=v (逆) |
| 容器II | 2.0×10-2 | 1.0×10-2 | 1.0×10-4 | 2.0×10-4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙烯能發生加成反應 | |
| B. | 乙烯易溶于水,也易溶于有機溶劑 | |
| C. | 可用酸性高錳酸鉀溶液鑒別乙烯與甲烷 | |
| D. | 乙烯的產量是衡量一個國家石油化工發展水平的標志 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
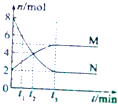 研究化學反應的快慢和限度具有十分重要的意義,請回答下列問題:
研究化學反應的快慢和限度具有十分重要的意義,請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com