

分析 實驗開始前要先打開A部分的活塞K1,持續通一段時間的氮氣再關閉K1,排盡裝置中的空氣,滴入濃硝酸反應生成二氧化氮和一氧化氮氣體,干燥后通過裝置C,在低于0℃時幾乎只有無色的N2O4液體或晶體存在,A中的反應停止后,打開D中的活塞K2,并通入氧氣,若反應確有NO產生,則D中出現紅棕色氣體,說明有一氧化氮氣體生成,剩余氣體用氫氧化鈉溶液吸收;
(1)根據銅和濃硝酸反應生成二氧化氮、硝酸銅和水,隨著反應的進行,硝酸濃度變稀,銅和稀硝酸反應生成一氧化氮氣體,硝酸銅和水;
(2)通入氮氣是排除裝置中的空氣,避免生成的一氧化氮氣體被氧化為二氧化氮;B裝置是利用濃硫酸的吸水性吸收氣體中的水蒸氣避免在C中 冷卻后水和二氧化氮反應生成一氧化氮;
(3)一氧化氮和氧氣反應生成紅棕色二氧化氮氣體;
(4)C裝置是冷卻氣體使二氧化氮轉化為四氧化二氮減少NO檢驗的干擾,E裝置除去尾氣防止倒吸、防止污染空氣;
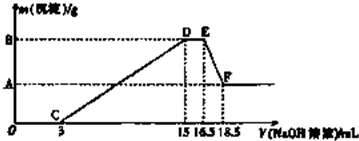
(5)硝酸的總的物質的量n=13.5mol•L1×0.04L=0.54mol,剩余硝酸n=1mol•L1×0.04L=0.04mol,確定反應的硝酸的物質的量;
(6)銅銀合金和硝酸全部反應生成銅鹽和銀鹽,利用A裝置中銀離子和氯離子形成的沉淀稱量計算得到合金中銅的質量分數.
解答 解:(1)銅和濃硝酸反應生成二氧化氮、硝酸銅和水,隨著反應的進行,硝酸濃度變稀,銅和稀硝酸反應生成一氧化氮氣體,硝酸銅和水,反應的可能化學方程式為:Cu+4HNO3(濃)=Cu(NO3)2+2NO2↑+2H2O、3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;
故答案為:Cu+4HNO3(濃)=Cu(NO3)2+2NO2↑+2H2O、3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;
(2)通入氮氣是排出裝置中的空氣,避免生成的一氧化氮氣體被氧化為二氧化氮;B裝置是利用濃硫酸的吸水性吸收氣體中的水蒸氣避免在C中冷卻后水和二氧化氮反應生成一氧化氮,
故答案為:排出系統的空氣,防止NO氧化為NO2;吸收水蒸氣,防止水蒸氣在C中冷凝后與NO2反應產生NO;
(3)A中的反應停止后,打開D中的活塞K2再通入氧氣,若反應中確有NO產生,一氧化氮和氧氣反應生成紅棕色氣體二氧化氮氣體;
故答案為:無色氣體變成紅棕色氣體;
(4)C裝置是冷卻氣體使二氧化氮轉化為四氧化二氮,盡量把NO2轉化為N2O4,減少對NO檢驗的干擾,E裝置除去尾氣NO2防止倒吸、防止污染空氣;
故答案為:盡量把NO2轉化為N2O4,減少對NO檢驗的干擾;除去NO2,防止污染空氣;
(5)硝酸的總的物質的量n=13.5mol•L1×0.02L=0.27mol,剩余硝酸n=1mol•L1×0.02L=0.02mol,所以參加反應的硝酸是0.27mol-0.02mol=0.25mol;
故答案為:0.25mol;
(6)銅銀合金和硝酸全部反應生成銅鹽和銀鹽,利用A裝置中銀離子和氯離子形成的氯化銀沉淀稱量,即在A中加入過量的Cl-的溶液,過濾、洗滌、干燥并稱量沉淀的質量,從而計算得到合金中銅的質量分數,
故答案為:在A中加入過量的Cl-的溶液,過濾、洗滌、干燥并稱量沉淀的質量.
點評 本題考查了物質性質的實驗設計,涉及硝酸性質,實驗步驟和產物性質及其反應現象是解題關鍵,題目難度中等.


 期末1卷素質教育評估卷系列答案
期末1卷素質教育評估卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | CH2Br-CH2Br 二溴乙烷 | B. | CH3OOCCH3乙酸甲酯 | ||
| C. |  硬脂酸甘油脂 硬脂酸甘油脂 | D. | 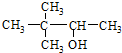 2,2-二甲基-3-丁醇 2,2-二甲基-3-丁醇 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 只有②④⑤ | B. | 只有⑤⑦ | C. | 只有①③⑦ | D. | 只有①② |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
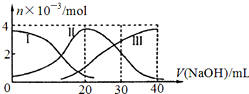
| A. | H2 A在水中的電離方程式是:H2A=H ++HA -;HA -═H++A2- | |
| B. | 當V(NaOH)=20mL時,則有:c(Na + )>c(HA- )>c(H + )>c(A 2- )>c(OH- ) | |
| C. | 當V(NaOH)=30mL時,則有:2c(H + )+c(HA- )+2c(H2A)=c(A 2- )+2 c(OH- ) | |
| D. | 當V(NaOH)=40mL時,其溶液中水的電離受到抑制 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3CH2Br$→_{水}^{NaOH}$ CH3CH2OH$→_{170℃}^{濃硫酸}$ CH2=CH2$\stackrel{Br_{2}}{→}$ CH2BrCH2Br | |
| B. | CH3CH2Br $\stackrel{HBr}{→}$ CH2BrCH2Br | |
| C. | CH3CH2Br $→_{水}^{NaOH}$ CH2=CH2 CH2BrCH3$\stackrel{HBr_{2}}{→}$CH2BrCH2Br | |
| D. | CH3CH2Br $→_{醇}^{NaOH}$ CH2=CH2$\stackrel{Br_{2}}{→}$ CH2BrCH2Br |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
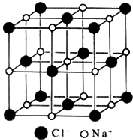
| A. | 在NaCl晶體中,每個Na+周圍與其距離最近的Na+有6個 | |
| B. | 氯離子采取A2密堆積,鈉離子填入八面體空隙中 | |
| C. | 每個晶胞含2個Na+和2個Cl- | |
| D. | 氯化鈉的化學式為NaCl |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com