
【題目】生產和實驗中廣泛采用甲醛法測定飽和食鹽水樣品中的NH4+含量。利用的反應原理為:4NH4++6HCHO=(CH2)6N4H+(一元酸)+3H++6H2O。實驗步驟如下:
①甲醛中常含有微量甲酸,應先除去。取甲醛amL于錐形瓶,加入1~2滴指示劑,用濃度為bmol/L的NaOH溶液滴定,滴定管的初始讀數為V1mL,當錐形瓶內溶液呈微紅色時,滴定管的讀數為V2mL。
②向錐形瓶加入飽和食鹽水試樣cmL,靜置1分鐘。
③用上述滴定管中剩余的NaOH溶液繼續滴定錐形瓶內溶液,至溶液呈微紅色時,滴定管的讀數為V3mL。
下列說法不正確的是
A.步驟①中的指示劑可以選用酚酞試液
B.步驟②中靜置的目的是為了使NH4+和HCHO完全反應
C.步驟②若不靜置會導致測定結果偏高
D.飽和食鹽水中的c(NH4+)=![]() mol/L
mol/L
【答案】C
【解析】
A. 酸和堿反應生成甲酸鈉,溶液呈堿性,步驟①中的指示劑可以選用酚酞試液,故A正確;
B. 通過延長反應時間,使反應進行得更充分,步驟②中靜置的目的是為了使NH4+和HCHO完全反應,故B正確;
C. 步驟②若不靜置,4NH4++6HCHO═(CH2)6N4H+(一元酸)+3H++6H2O,反應不完全,生成的酸少,會導致測定結果偏低,故C錯誤;
D. 除去甲酸后的氫氧化鈉溶液讀數為V2 mL,加入飽和食鹽水試樣c mL,再加1~2滴酚酞,再用上述NaOH溶液滴定至微紅色,滴定管的讀數V3 mL,此時4NH4++6HCHO═(CH2)6N4H+(一元酸)+3H++6H2O,滴入氫氧化鈉反應,4NH4++~((CH2)6N4H+(一元酸)+3H+)~4OH-;氫氧化鈉物質的量和氮元素物質的量相同,所以飽和食鹽水中的c(NH4+)=![]() =
=![]() mol·L-1,故D正確;
mol·L-1,故D正確;
故選C。


科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A. 乳酸薄荷醇酯(![]() )僅能發生水解、氧化、消去反應
)僅能發生水解、氧化、消去反應
B. 乙醛和丙烯醛(![]() )不是同系物,它們與氫氣充分反應后的產物也不是同系物
)不是同系物,它們與氫氣充分反應后的產物也不是同系物
C. 用核磁共振氫譜不能區分HCOOCH3和HCOOCH2CH3
D. 分子式為C9H12的苯的同系物,若苯環上只有一個取代基,則其一溴代物最多有6種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一密閉容器中通入A、B、C三種氣體,保持一定溫度,在t1~t4s時測得各物質的濃度如表,則下列判斷正確的是
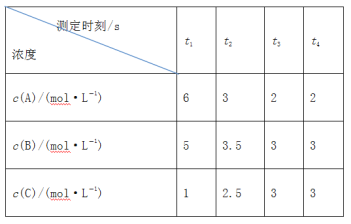
A.在t3s時反應已經停止
B.t3~t4s內正、逆反應速率不相等
C.在容器中發生的反應為A(g)+B(g)![]() C(g)
C(g)
D.在t2~t3s內A的平均反應速率為![]() mol·L1·s1
mol·L1·s1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關實驗室制取氣體的反應中,其反應不屬于氧化還原反應的是( )
A.實驗室中用稀硫酸與Mg反應制取H2B.實驗室中用高錳酸鉀加熱分解制取O2
C.實驗室中用H2O2與MnO2作用產生O2D.實驗室中用稀鹽酸與石灰石反應制取CO2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】資料顯示:FeF3溶液接近無色。某同學據此進行以下實驗,依據上述實驗無法獲得的結論是
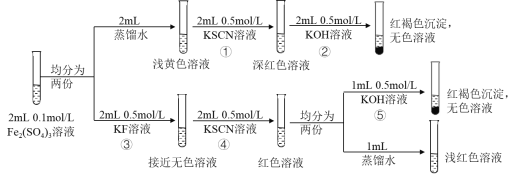
A.FeF3是弱電解質
B.④中發生的離子反應為FeF3+3SCN-Fe(SCN)3+3F-
C.相同條件下,結合Fe3+的能力:SCN->F->OH-
D.向Fe(SCN)3溶液中加入NaF固體,溶液顏色會變淺
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,可逆反應C(s)+CO2(g)![]() 2CO(g),達到平衡狀態,現進行如下操作:①升高反應體系的溫度;②增加反應物C的用量;③縮小反應體系的體積:④減少體系中CO的量。上述措施中一定能使反應的正反應速率顯著加快的是( )
2CO(g),達到平衡狀態,現進行如下操作:①升高反應體系的溫度;②增加反應物C的用量;③縮小反應體系的體積:④減少體系中CO的量。上述措施中一定能使反應的正反應速率顯著加快的是( )
A.①②③④B.①③
C.④②D.①③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖為原電池裝置示意圖:
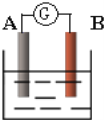
(1)若A為Zn,B為石墨棒,電解質溶液為稀硫酸,則A為_______極(填正或負),寫出電極反應式:正極_______,負極_______.總反應離子方程式為:_______。
(2)若A為銅片,B為鐵片,電解質為FeCl3溶液,則A為_______極(填正或負),寫出電極反應式:正極_______,負極_______.總反應離子方程式為:_______。
(3)若A、B均為鉑片,電解質為KOH溶液,分別從A、B兩極通入H2和O2,該電池即為燃料電池,通入氧氣的一極為該電池的_______極(填正或負),寫出電極反應式:正極______________,負極______.總反應方程式為:______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25 ℃時,將 0.10 mol·L-1 CH3COOH 溶液滴加到 10 mL 0.10 mol·L-1 NaOH 溶液中,lg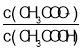 與pH 的關系如圖所示,C 點坐標是(6,1.7)。下列說法不正確的是
與pH 的關系如圖所示,C 點坐標是(6,1.7)。下列說法不正確的是
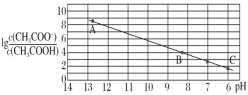
A.pH=7 時加入的醋酸溶液的體積大于 10 mL
B.C 點后繼續加入醋酸溶液,水的電離程度減小
C.B 點存在 c(Na+)-c(CH3COO-)=(10-6-10-8)mol·L-1
D.Ka(CH3COOH)=10-4.3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列指定反應的離子方程式正確的是
A. Cl2與H2O的反應:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
B. 銅絲插入Fe2(SO4)3溶液中:Cu +Fe3+ =Cu2+ +Fe2+
C. 向FeBr2溶液中通入過量Cl2:2Br-+Cl2=Br2+2Cl-
D. 向Na2SiO3溶液中通入過量CO2:SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3—
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com