
張明同學在學習“硫酸及其鹽的某些性質(zhì)與用途”中,進行如下實驗探究.
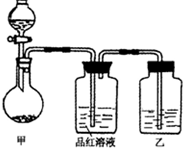
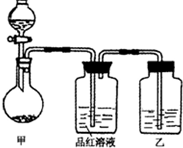
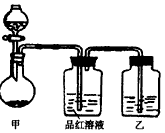
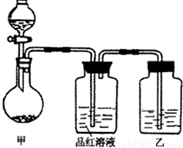
[實驗一]探究濃硫酸的氧化性:將實驗室常用的藥品放入如圖所示的實驗裝置后,加熱裝置甲.(夾持和加熱裝置省略)

(1)該裝置設計上存在明顯缺陷,請指出:________.
(2)寫出裝置甲中反應的化學方程式:________.
(3)裝置乙中的試劑是________.
[實驗二]探究某硫酸亞鐵鹽固體是否變質(zhì)
(4)請你幫助張明同學完成如下實驗方案:
[實驗三]用KHSO4制取H2O2并測其質(zhì)量分數(shù)
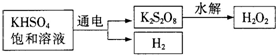
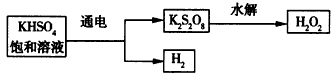
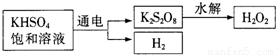
查閱資料得知:工業(yè)上用電解KHSO4飽和溶液制取H2O2,示意圖如下:
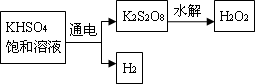
張明用此法制取一定濃度的H2O2,并進行下列實驗測定H2O2的質(zhì)量分數(shù):
(離子方程式:2MnO4―+5H2O2+6H+![]() 2Mn2++8H2O+5O2↑)
2Mn2++8H2O+5O2↑)
①取5.00 mL H2O2溶液(密度為1.00 g/mL)置于錐形瓶中加水稀釋,再加稀硫酸酸化;
②用0.1000 mol/L KMnO4溶液滴定;
③用同樣方法滴定,三次消耗KMnO4溶液的體積分別為20.00 mL、19.98 mL、20.02 mL.
回答下列問題:
(5)電解飽和KHSO4溶液時,陽極的電極反應式為________.
(6)操作②中,滴入第一滴KMnO4溶液,溶液紫紅色消失很慢,隨著滴定過程中Mn2+的增多,溶液紫紅色消失速率加快.Mn2+的作用是________.
(7)原H2O2溶液中溶質(zhì)的質(zhì)量分數(shù)為________.
科目:高中化學 來源: 題型:閱讀理解
 (2009?三明一模)張明同學在學習“硫酸及其鹽的某些性質(zhì)與用途“中,進行如下實驗探究.
(2009?三明一模)張明同學在學習“硫酸及其鹽的某些性質(zhì)與用途“中,進行如下實驗探究.
| ||
| ||
| ||
| ||
| 實驗操作 | 預期現(xiàn)象和結論 |
往一支試管中加入少量固體,加水溶解,再滴加幾滴KSCN溶液 往一支試管中加入少量固體,加水溶解,再滴加幾滴KSCN溶液 |
若溶液變?yōu)榧t色,說明該固體已變質(zhì);若溶液未變紅色,說明該固體沒有變質(zhì) 若溶液變?yōu)榧t色,說明該固體已變質(zhì);若溶液未變紅色,說明該固體沒有變質(zhì) |

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 張明同學在學習“硫酸及其鹽的某些性質(zhì)與用途“中,進行如下實驗探究.
張明同學在學習“硫酸及其鹽的某些性質(zhì)與用途“中,進行如下實驗探究.| 實驗操作 | 預期現(xiàn)象和結論 |
| ______ | ______ |

查看答案和解析>>
科目:高中化學 來源:三明一模 題型:填空題
| 實驗操作 | 預期現(xiàn)象和結論 |
| ______ | ______ |
查看答案和解析>>
科目:高中化學 來源:遼寧省模擬題 題型:實驗題

查看答案和解析>>
科目:高中化學 來源:2009年福建省三明市高考化學一模試卷(解析版) 題型:填空題
| 實驗操作 | 預期現(xiàn)象和結論 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com