
| 0.322 |
| 0.84×0.082 |


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:

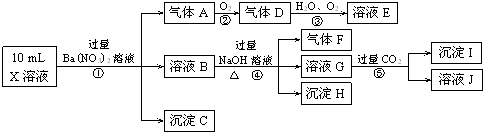
| A、氣體甲一定是純凈物 |
| B、沉淀乙為Mg(OH)2 |
| C、沉淀甲是硅酸和硅酸鎂的混合物 |
| D、溶液X中一定存在K+、AlO2-和SiO32-離子 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、△H3=△H1+2△H2 |
| B、△H3=△H1+△H2 |
| C、△H3=△H1-2△H2 |
| D、△H3=△H1-△H2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 2 |
| 3 |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
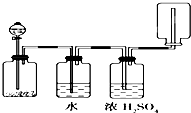
| A、KMnO4分解生成氧氣 |
| B、二氧化錳和鹽酸生產氯氣 |
| C、碳酸鈣和鹽酸生成二氧化碳 |
| D、鋅和鹽酸生成氫氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com