

 溶液出現藍色且30s內不褪色
溶液出現藍色且30s內不褪色分析 (一)(1)燒瓶A中亞硫酸鈉與硫酸反應生成二氧化硫、硫酸鈉和水;D可防止液體倒吸;
(2)觀察SO2的生成速率,則溶液不能與SO2反應;
(3)燒杯、錐形瓶需要加熱時必須使用石棉網,蒸發皿、試管可直接加熱;
(4)由題目信息可知,硫代硫酸鈉(Na2S2O3)遇酸易分解,而二氧化硫過量會使溶液呈酸性;
(二)(5)NaHSO3溶液中HSO3-的電離程度大于水解程度,溶液呈酸性,故檢驗溶液呈酸性即可;
(6)由消耗碘的量,結合SO2+I2+2H2O═H2SO4+2HI計算二氧化硫的質量,進而計算濃度;若有部分HI被空氣氧化,則消耗碘的量偏小,故測定二氧化硫的量偏小.
解答 解:(1)燒瓶A中亞硫酸鈉與硫酸反應生成二氧化硫、硫酸鈉和水,其反應的離子方程式為:SO32-+H2SO4=SO42-+SO2↑+H2O;D中左側為短導管可防止液體倒吸;
故答案為:SO32-+H2SO4=SO42-+SO2↑+H2O;防止倒吸;
(2)觀察SO2的生成速率,是通過觀察溶液中產生氣泡的快慢來判斷,所以溶液不能與SO2反應,選項中只有飽和NaHSO3溶液與二氧化硫不反應,
故答案為:c;
(3)體積較大的玻璃儀器在加熱時,儀器下面要放石棉網,防止儀器受熱不均而炸裂,其中燒杯、錐形瓶加熱時必須使用石棉網,
故答案為:ad;
(4)由題目信息可知,硫代硫酸鈉(Na2S2O3)遇酸易分解,若二氧化硫過量會使溶液呈酸性,故實驗中通入的SO2不能過量,防止硫代硫酸鈉分解,
故答案為:若二氧化硫過量會使溶液呈酸性,使硫代硫酸鈉發生分解;
(二)(5)NaHSO3溶液中HSO3-的電離程度大于水解程度,溶液呈酸性,測定溶液的pH,可以確定溶液酸堿性,酸性溶液可以使濕潤藍色石蕊試紙變紅,所以能用測定溶液pH值、濕潤的藍色石蕊試液檢驗,而加入Ba(OH)2溶液、HCl溶液、品紅溶液都不能說明溶液呈酸性,故選ae;
故答案為:ae;
(6)令100mL葡萄酒中二氧化硫的質量為mg,則:
SO2+2H2O+I2═H2SO4+2HI
64g 1mol
mg 0.025L×0.01mol/L
所以$\frac{64g}{mg}$=$\frac{1mol}{0.025L×0.01mol/L}$,
解得m=0.016,
故該次實驗測得樣品中抗氧化劑的殘留量(以游離SO2計算)為$\frac{0.016g}{0.1L}$=0.16 g/L;
若有部分HI被空氣氧化,則消耗碘的量偏小,故測定二氧化硫的量偏小,則測定結果偏低;HI與氧氣反應的化學方程式為:4HI+O2=2I2+2H2O;
故答案為:0.16;偏低;4HI+O2=2I2+2H2O.
點評 本題考查物質的制備實驗、實驗方案設計、物質含量的測定、氧化還原反應滴定等,難度中等,明確實驗原理是解本題關鍵,根據物質的性質分析解答,注意元素化合物知識的積累和靈活運用.


科目:高中化學 來源: 題型:解答題
| 化學鍵 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
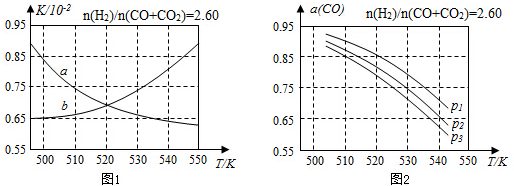
 | 0.600 | 0.500 | 0.400 | 0.300 |
| 318.2 | 3.60 | 3.00 | 2.40 | 1.80 |
| 328.2 | 9.00 | 7.50 | a | 4.50 |
| b | 2.16 | 1.80 | 1.44 | 1.08 |
| A. | a=6.00 | |
| B. | 同時改變反應溫度和蔗糖的濃度,v可能不變 | |
| C. | b<318.2 | |
| D. | 不同溫度時,蔗糖濃度減少一半所需的時間相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 利用LiOH和鈷氧化物可制備鋰離子電池正極材料.LiOH可由電解法制備,鈷氧化物可通過處理鈷渣獲得.
利用LiOH和鈷氧化物可制備鋰離子電池正極材料.LiOH可由電解法制備,鈷氧化物可通過處理鈷渣獲得.
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
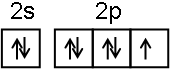 ;NF3中心原子軌道的雜化類型為sp3.
;NF3中心原子軌道的雜化類型為sp3.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | c(OH-)=c(Na+)+c(H+) | |
| B. | 該溶液中的c(OH-)=1.0×10-3mol•L-1 | |
| C. | 加水稀釋104倍所得溶液顯堿性 | |
| D. | 與pH=3的HF溶液等體積混合所得溶液:c(Na+)=c(F-)+c(HF) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cl2通入Na2CO3溶液中 | B. | CO2通入CaCl2溶液中 | ||
| C. | NH3通入AgNO3溶液中 | D. | SO2通入NaHS溶液中 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
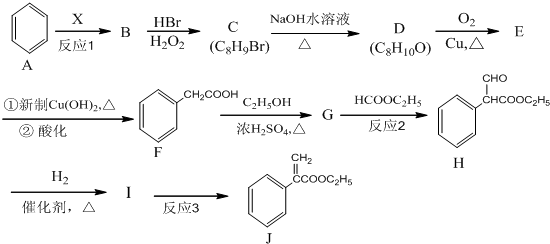
 ,G的結構簡式為
,G的結構簡式為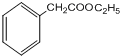 .
.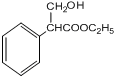

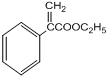 +H2O.
+H2O.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH4+、Al3+、NO3-、AlO2- | B. | Na+、Fe3+、HSO3-、OH- | ||
| C. | Cu2+、NH4+、SO42-、Cl- | D. | K+、H+、I-、ClO- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com