
【題目】汽車用汽油的抗爆劑約含 17%的 1,2一二溴乙烷。某學習小組用下圖所示裝置制備少量 1,2 一二溴乙烷,具體流秳如下: 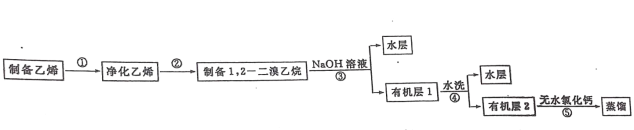
已知:1,2 一二溴乙烷的沸點為131℃,熔點為9.3℃。Ⅰ1,2 一二溴乙烷的制備步聚①、②的實驗裝置為:
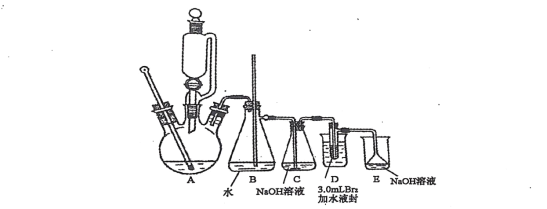
實驗步驟:
(ⅰ)在冰水冷卻下,將 24mL 濃硫酸慢慢注入12mL乙醇中混合均勻。
(ⅱ)向 D 裝置的試管中加入3.0mL 液溴(0.10mol),然后加入適量水液封,幵向燒杯中加入冷卻劑。
(ⅲ)連接儀器并檢驗氣密性。向三口燒瓶中加入碎瓷片,通過滴液漏斗滴入一部分濃硫酸與乙醇的混合物,一部分留在滴液漏斗中。
(ⅳ)先切斷瓶C與瓶D的連接處,加熱三口瓶,待溫度上升到約120℃,連接瓶 C與瓶D,待溫度升高到180~200℃,通過滴液漏斗慢慢滴入混合液。
(V)繼續加熱三口燒瓶,待D裝置中試管內的顏色完全褪去,切斷瓶C與瓶D的連接處,再停止加熱。回答下列問題:
(1)圖中 B 裝置玻璃管的作用為__________________________________________。
(2)(ⅳ)中“先切斷瓶C與瓶D的連接處,再加熱三口瓶”的原因是__________________________________________。
(3)裝置D的燒杯中需加入冷卻劑,下列冷卻劑合適的為__________________________________________。
a.冰水混合物 b.5℃的水 c.10℃的水
Ⅱ1,2 一二溴乙烷的純化
步驟③:冷卻后,把裝置 D 試管中的產物轉移至分液漏斗中,用 1%的氫氧化鈉水溶液洗滌。
步驟④:用水洗至中性。
步驟⑤:“向所得的有機層中加入適量無水氯化鈣,過濾,轉移至蒸餾燒瓶中蒸餾,收集
130~132℃的餾分,得到產品5.64g。
(4)步驟③中加入 1%的氫氧化鈉水溶液時,發生反應的離子方程式為__________________________________________。
(5)步驟⑤中加入無水氯化鈣的作用為_________________________。該實驗所得產品的產率為__________________________________________。
【答案】指示 B 中壓強變化,避免氣流過快引起壓強過大 防止乙烯生成前裝置中的熱氣體將溴吹出而降低產率 c Br2+2OH-=Br-+BrO-+H2O 干燥產品(除去產品中的水) 30%
【解析】
(1)圖中B裝置氣體經過,但B中氣體流速過快,則壓強會過大,通過觀察B中玻璃管可以看出氣體的流速和反應速率,因此玻璃管的作用為指示B中壓強變化,避免氣流過快引起壓強過大。
(2)(ⅳ)中“先切斷瓶C與瓶D的連接處,再加熱三口瓶”的原因是防止乙烯生成前裝置中的熱氣體將溴吹出而降低產率。
(3)裝置D的燒杯中需加入冷卻劑,因為1,2一二溴乙烷的沸點為131℃,熔點為9.3℃,因此只能讓1,2一二溴乙烷變為液體,不能變為固體,變為固體易堵塞導氣管,因此合適冷卻劑為c。
(4)步驟③中加入1%的氫氧化鈉水溶液主要是將1,2一二溴乙烷中的單質溴除掉,發生反應的離子方程式為Br2+2OH-=Br-+BrO-+H2O。
(5)步驟⑤中加入無水氯化鈣的作用為干燥產品(除去產品中的水);單質溴為0.1mol,根據質量守恒得到1,2一二溴乙烷理論物質的量為0.1mol,因此該實驗所得產品的產率為![]() 。
。
(1)圖中B裝置氣體經過,但B中氣體流速過快,則壓強會過大,通過觀察B中玻璃管可以看出氣體的流速和反應速率,因此玻璃管的作用為指示B中壓強變化,避免氣流過快引起壓強過大,故答案為:指示B中壓強變化,避免氣流過快引起壓強過大。
(2)(ⅳ)中“先切斷瓶C與瓶D的連接處,再加熱三口瓶”的原因是防止乙烯生成前裝置中的熱氣體將溴吹出而降低產率,故答案為:防止乙烯生成前裝置中的熱氣體將溴吹出而降低產率。
(3)裝置D的燒杯中需加入冷卻劑,因為1,2一二溴乙烷的沸點為131℃,熔點為9.3℃,因此只能讓1,2一二溴乙烷變為液體,不能變為固體,變為固體易堵塞導氣管,因此合適冷卻劑為c,故答案為:c。
(4)步驟③中加入1%的氫氧化鈉水溶液主要是將1,2一二溴乙烷中的單質溴除掉,發生反應的離子方程式為Br2+2OH-=Br-+BrO-+H2O,故答案為:Br2+2OH-=Br-+BrO-+H2O。
(5)步驟⑤中加入無水氯化鈣的作用為干燥產品(除去產品中的水);單質溴為0.1mol,根據質量守恒得到1,2一二溴乙烷理論物質的量為0.1mol,因此該實驗所得產品的產率為![]() ,故答案為:干燥產品(除去產品中的水);30%。
,故答案為:干燥產品(除去產品中的水);30%。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】碳、氫、氧三種元素組成的有機物A,相對分子質量為152,其分子中碳、氫原子個數比為1:1,含氧元素的質量分數為31.58%。A遇FeCl3溶液顯紫色,其苯環上的一氯取代物有兩種,請回答下列問題:
(1)A的分子式是__。
(2)寫出A與NaHCO3溶液反應的化學方程式:__。
(3)若A可以發生如圖所示轉化關系,D的分子式為C10H12O3,寫出D的結構簡式__。

(4)甲、乙兩裝置均可用作實驗室由C制取B的裝置,乙圖采用甘油浴加熱(甘油沸點290℃,熔點18.17℃),當甘油溫度達到反應溫度時,將盛有C和濃硫酸混合液的燒瓶放入甘油中,很快達到反應溫度。甲、乙兩裝置相比較,乙裝置有哪些優點___?

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下用pH為3的某酸溶液分別與pH都為11的氨水、氫氧化鈉溶液等體積混合得到a、b兩種溶液,關于這兩種溶液酸堿性的描述正確的是![]()
![]()
A.b一定顯中性B.b可能顯堿性或酸性
C.a不可能顯酸性D.a可能顯酸性或堿性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】分枝酸可用于生化研究。其結構簡式如圖。下列關于分枝酸的敘述正確的是

A. 分子中含有2種官能團
B. 可與乙醇、乙酸反應,且反應類型相同
C. 1mol分枝酸最多可與3molNaOH發生中和反應
D. 可使溴的四氯化碳溶液、酸性高錳酸鉀溶液褪色,且原理相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學習小組查閱資料,設計以下流程驗證 SO2 的還原性。
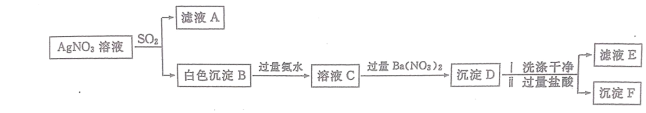
已知:沉淀 D 洗滌干凈,加入過量鹽酸時,部分沉淀溶解,剩余少量沉淀 F。(1)關于“白色沉淀 B”的成份
①甲同學推斷白色沉淀 B 含 Ag2SO4。
實驗現象依據:“沉淀 F”說明“沉淀 D”中含________________ (填化學式),進而說明“白色沉淀B"中含 Ag2SO4。
②乙同學認為“白色沉淀 B”中含有 Ag2SO3。
實驗現象依據:“沉淀 D 洗滌干凈,加入過量鹽酸時,部分沉淀溶解”,溶解的物質為 BaSO3, 進而推斷沉淀 B 中含 Ag2SO3。為進一步證實 B 中含有 Ag2SO3,可取少量濾液 E于試管中加入少量________________,有白色沉淀生成。
(2)常溫下,Ag2SO4 與 Ag2SO3 中 c(Ag+)與 c(SO32-)的關系如下圖所示:
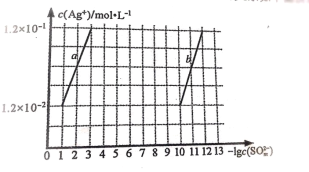
已知:Ksp(Ag2SO4)>Ksp(Ag2SO3),回答問題:
①表示 Ag2SO4 的沉淀溶解平衡關系的曲線是________________ (填“a”、“b”)
②Ksp(Ag2SO3)為________________mol3L-3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,已知某三元弱酸H3A的三級電離平衡常數分別為![]() 、
、![]() 、
、![]() ,下列說法錯誤的是
,下列說法錯誤的是
A.Na3A的第一級水解平衡常數Kh1的數量級為10-2
B.在NaH2A溶液中:![]()
C.0.1mol/L的Na3A和0.1mol/L的Na2HA溶液中水電離程度,前者大于后者
D.向H3A溶液中加入NaOH溶液至中性時:c(Na+)=3c(A3-)+2c(HA2-)+c(H2A-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關實驗原理、現象、結論均正確的是( )
A. 圖中滴加乙醇,試管中橙色溶液變為綠色,說明
圖中滴加乙醇,試管中橙色溶液變為綠色,說明![]() 被還原成
被還原成![]()
B. 圖中,右邊試管中產生氣泡迅速,說明氯化鐵的催化效果比二氧化錳好
圖中,右邊試管中產生氣泡迅速,說明氯化鐵的催化效果比二氧化錳好
C. 圖中,由試管中收集到的無色氣體,證明銅與稀硝酸的反應產物是NO
圖中,由試管中收集到的無色氣體,證明銅與稀硝酸的反應產物是NO
D. 圖中,試管中先出現白色沉淀、加
圖中,試管中先出現白色沉淀、加![]() 后產生黑色沉淀,但不能驗證AgCl的溶解度大于
后產生黑色沉淀,但不能驗證AgCl的溶解度大于![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用鈦白粉廠廢酸(主要含硫酸、Fe3+、Fe2+、TiO2+、Al3+)制備過二硫酸銨[(NH4)2S2O8],同時回收TiO(OH)2的簡要流程如下:
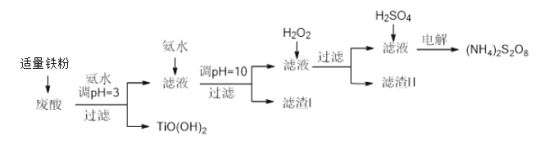
已知:i.部分離子完全生成氫氧化物沉淀的pH:
金屬離子 | TiO2+ | Fe3+ | Fe2+ | Al3+ |
開始沉淀的PH | 1.2 | 1.9 | 7.0 | 3.2 |
沉淀完全的pH | 2.8 | 3.1 | 9.4 | 4.7 |
ii.pH>7時,Fe2+部分生成Fe(II)氨絡離子[Fe(NH3)2]2+。
請回答下列問題:
(1)加入適量鐵的作用是________________________。
(2)生成TiO(OH)2的化學方程式是____________________。
(3)濾渣I、濾渣Ⅱ中均含有的物質的化學式是________
(4)加入H2O2的目的是氧化除掉Fe(II)氨絡離子[Fe(NH3)2]2+,配平下列離子方程式:2[Fe(NH3)2]2++____________+4H2O +H2O2=___________+ 4NH3·H2O。
(5)常溫下,電解液中含硫微粒主要存在形式與pH的關系如下圖所示。
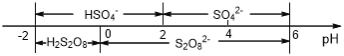
在陽極放電的離子主要為HSO4-,陽極區電解質溶液的pH范圍為_________
(6)已知Ksp[Al(OH)3]=3.2×10-34 ,當pH=10 時,求溶液中c(Al3+)=___________
(7)25℃,pH=3的(NH4)2SO4溶液中,計算2c(SO42-)- c(NH4+) =___________(列式即可)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是用于航天飛行器中的一種全天候太陽能電化學電池在光照時的工作原理。下列說法正確的是

A.夜間無光照時,a電極流出電子
B.光照時,H+由a極室通過質子膜進入b極室
C.光照時,b極反應式是VO2++2OH--e-=VO2++H2O
D.該電池與硅太陽能電池供電原理相同
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com