
| A. | LiCl | B. | NaCl | C. | KCl | D. | KBr |
分析 兩離子間距=陽離子半徑+陰離子半徑.而離子的電子層數越多,離子半徑越大;當電子層數相同時,核電荷數越多,半徑越小;以此來解答.
解答 解:在LiCl、NaCl、KCl三種物質中,陰離子相同,故離子間的距離取卻于陽離子,而Li+的核外有1個電子層,Na+的核外有2個電子層,K+的核外有3個電子層,故三種物質中KCl中離子間距最大;而KCl和KBr的陽離子相同.陰離子不同,故離子間距大小取決于陰離子,而Br-的核外有4個電子層,故半徑大于Cl-,則KBr中的離子間距大于KCl中的離子間距,故選D.
點評 本題考查了依托離子間距的大小比較來考查了離子半徑的大小比較,應注意的是比較離子半徑時,先考慮電子層數,然后考慮核電荷數,最后考慮電子數.


 天天練口算系列答案
天天練口算系列答案科目:高中化學 來源: 題型:選擇題
| A. | 227.2kJ•mol-1 | B. | -227.2kJ•mol-1 | C. | 798.8kJ•mol-1 | D. | -798.8kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗操作 | 現象 | 結論 |
| A | 測定常溫時的等濃度的HCOONa溶液、CH3COONa溶液的pH | pH(HCOONa)<pH(CH3COONa) | 弱酸的酸性:HCOOH>CH3COOH |
| B | 向0.5ml 2mol/L的NaOH溶液中加入1ml 1mol/L的CuSO4溶液,振蕩后再加入0.5ml有機物X,加熱 | 未出現磚紅色沉淀 | 說明X中不含有醛基 |
| C | KBrO3溶液中加入少量苯,然后通入少量Cl2 | 有機相呈橙紅色 | 氧化性:Cl2>Br2 |
| D | NaAlO2溶液與NaHCO3溶液混合 | 有白色絮狀沉淀生成 | 二者水解相互促進生成氧化鋁沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,15g甲基(-CH3)所含的中子數為6NA | |
| B. | a gO2和O3的混合氣體中含有的分子總數為$\frac{a{N}_{A}}{32}$ | |
| C. | 在1L的碳酸鈉溶液中,若c(CO32-)=1mol•L-1,則Na+個數為2NA | |
| D. | 78g過氧化鈉晶體中,含2NA個陰離子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe3+ | B. | HNO3 | C. | Cl2 | D. | MnO4- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 A、B、C、D、E分別是鐵或鐵的化合物,其中D是一種紅褐色沉淀,其相互反應關系如圖所示:
A、B、C、D、E分別是鐵或鐵的化合物,其中D是一種紅褐色沉淀,其相互反應關系如圖所示:查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| 操作和現象(或數據) | 結論 | |
| A | 向盛有1 mL 0.1 mol/L MgCl2溶液試管中加1 mL 0.2 mol/L NaOH溶液,有白色沉淀生成,再加入2滴0.1mol/LFeCl3溶液,又生成紅褐色沉淀 | 溫度相同時,Fe(OH)3溶解度小于Mg(OH)2 |
| B | 向含有少量氫氧化鎂沉淀的試管中滴入NH4Cl溶液,沉淀逐漸溶解,并有刺激性的氣味氣體產生 | 對應的離子反應方程式為NH4++OH-═NH3↑+H2O- |
| C | 20克Ba(OH)2•8H2O粉末和10克NH4Cl粉末混合后玻璃棒迅速攪拌,可以聞到刺激性氣味的氣體 | 該反應為放熱反應,促使氨水分解生成NH3 |
| D | 常溫下,將NaAlO2溶液和NaHCO3溶液混合產生大量白色沉淀 | 說明AlO2-結合H+能力大于CO32- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
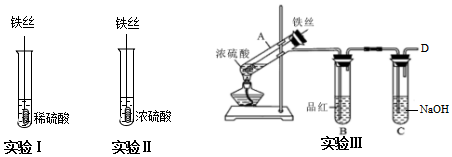
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com