
| A. | 金屬銅與濃硝酸或稀硝酸反應 | |
| B. | 鈉在常溫或加熱條件與氧氣反應 | |
| C. | 鐵在少量氯氣或過量的氯氣中點燃 | |
| D. | 氯化鋁溶液與少量氫氧化鈉溶液或過量氫氧化鈉溶液反應 |
分析 A.Cu與濃硝酸反應生成二氧化氮,與稀硝酸反應生成NO;
B.常溫生成氧化鈉,加熱生成過氧化鈉;
C.鐵在少量氯氣或過量的氯氣中點燃,均生成氯化鐵;
D.與少量NaOH反應生成氫氧化鋁,與過量NaOH反應生成偏鋁酸鈉.
解答 解:A.Cu與濃硝酸反應生成二氧化氮,與稀硝酸反應生成NO,反應產物不同,故A不選;
B.常溫生成氧化鈉,加熱生成過氧化鈉,反應產物與條件有關,產物不同,故B不選;
C.鐵在少量氯氣或過量的氯氣中點燃,均生成氯化鐵,反應產物與量無關,產物相同,故C選;
D.與少量NaOH反應生成氫氧化鋁,與過量NaOH反應生成偏鋁酸鈉,反應產物與量有關,產物不同,故D不選;
故選C.
點評 本題考查金屬及化合物的性質,為高頻考點,把握元素化合物的性質及發生的反應為解答的關鍵,側重分析與應用能力的考查,注意與量有關的反應及反應條件對反應的影響,題目難度不大.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4 LHF中分子總數為NA | |
| B. | 室溫下,31.0g白磷中含有的共價鍵數目為1.5NA | |
| C. | 常溫常壓下,17 g甲基(-14CH3)所含的電子數為9NA | |
| D. | .將1molCl2通入到水中,則N(HClO)+N(Cl-)+N(ClO-)=2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 需要加熱才能發生的反應一定是吸熱反應 | |
| B. | 1mol甲烷燃燒生成水蒸汽和二氧化碳所放出的熱量就是甲烷的燃燒熱 | |
| C. | CO(g)的燃燒熱△H=-283.0kJ/mol,則2CO2(g)=2CO(g)+O2(g)的反應熱△H=+566.0kJ/mol | |
| D. | 已知中和熱△H=-57.3kJ/mol,則稀H2SO4和Ba(OH)2溶液反應生成2molH2O的反應熱△H=-114.6kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1.0mol/L的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| B. | 與鋁反應產生大量氫氣的溶液:Na+、K+、CO32-、Cl- | |
| C. | 飽和新制氯水中:Na+、K+、NO3-、I- | |
| D. | 使酚酞試液變紅的溶液:Na+、K+、SiO32-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2.25mol/L | B. | 2mol/L | C. | 4mol/L | D. | 0.6mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
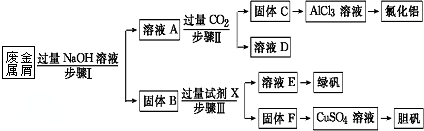
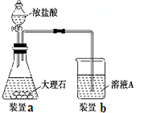 一段時間后,觀察到燒杯中產生的白色沉淀會逐漸減少.為了避免固體C減少,可采取的改進措施是在裝置I和Ⅱ之間增加一個盛有飽和NaHCO3溶液的洗氣瓶
一段時間后,觀察到燒杯中產生的白色沉淀會逐漸減少.為了避免固體C減少,可采取的改進措施是在裝置I和Ⅱ之間增加一個盛有飽和NaHCO3溶液的洗氣瓶
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com