
| A. | 所含質子數=A-n | B. | 所含中子數=A-Z | C. | 所含電子數=Z+n | D. | 質量數=Z+A |
分析 根據元素符號的左下角表示質子數,左上角表示質量數,右上角為所帶電荷數,右下角為原子個數,中子數=質量數-質子數,核電荷數=質子數=原子序數.陽離子中核外電子數=質子數-電荷數.
解答 解:AZRn-中質子數為Z,質量數為A,中子數=質量數-質子數=A-Z,核電荷數=Z,電荷數為n-,該微粒是陽離子,所以核外電子數=質子數-電荷數=Z-n.
A.所含質子數=A-N,故A錯誤;
B.所含中子數=A-Z,故B正確;
C.所含電子數=Z-n,故C錯誤;
D.質量數為A,故D錯誤;
故選:B.
點評 本題考查了質子數、質量數、中子數、核外電子數之間的關系,難度不大,明確各物理量之間的關系是解本題的關鍵.


 津橋教育計算小狀元系列答案
津橋教育計算小狀元系列答案科目:高中化學 來源: 題型:多選題
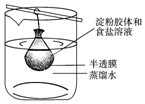 將10mL淀粉膠體和5mL氯化鈉溶液混合后,放入用半透膜制成的袋內,將此袋浸入蒸餾水中(如圖所示)2min后,分別取袋內和燒杯內液體進行實驗.下列說法正確的是( )
將10mL淀粉膠體和5mL氯化鈉溶液混合后,放入用半透膜制成的袋內,將此袋浸入蒸餾水中(如圖所示)2min后,分別取袋內和燒杯內液體進行實驗.下列說法正確的是( )| A. | 燒杯內液體加入硝酸銀溶液后有白色沉淀產生 | |
| B. | 燒杯內液體加入碘水后呈藍色 | |
| C. | 袋內液體加入硝酸銀溶液后不會出現白色沉淀 | |
| D. | 袋內液體加入碘水后不變藍 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | p(N2)>p(H2)>p(O2) | B. | p(O2)>p(N2)>p(H2) | C. | p(N2)>p(O2)>p(H2) | D. | p(H2)>p(N2)>p(O2) |
查看答案和解析>>
科目:高中化學 來源:2016-2017學年云南省高一9月月考化學卷(解析版) 題型:選擇題
對于反應3Cl2+6NaOH=5NaCl+NaClO3+3H2O,以下敘述正確的是
A.Cl2是氧化劑,NaOH是還原劑
B.每生成1個的NaClO3轉移10個的電子
C.Cl2既是氧化劑又是還原劑
D.被氧化的Cl原子和被還原的Cl原子之比為5∶1
查看答案和解析>>
科目:高中化學 來源:2016-2017學年云南省高一9月月考化學卷(解析版) 題型:選擇題
已知某酸性溶液中含有Ba2+、Fe3+,則下述離子組 中能與上述離子大量共存的
中能與上述離子大量共存的
A.CO32-、Cl- B.NO3-、Cl- C.NO3-、SO42- D.OH-、NO3-
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向FeCl3溶液中加入少量鋅粒:2Fe3++Zn═2Fe2++Zn2+ | |
| B. | 向Ba(NO3)2溶液中通入SO2氣體,出現白色沉淀:Ba2++SO2+H2O═BaSO3↓+2H+ | |
| C. | 向H2O2溶液中滴加酸化的KMnO4溶液,KMnO4溶液褪色:2MnO4-+7H2O2+6H+═2Mn2++6O2↑+10H2O | |
| D. | 向FeCl3溶液中加入少量Na2S溶液:2Fe3++3S2-═Fe2S3↓ |
查看答案和解析>>
科目:高中化學 來源:2016-2017學年云南省高一9月月考化學卷(解析版) 題型:選擇題
對四種無色溶液進行離子檢驗,實驗結果如下,其中明顯錯誤的是
A.K+、Na+、Cl-、NO3- B.K+、NO3-、OH-、CO32-
C.Na+、OH-、Cl-、NO3- D.MnO4-、K+、S2-、Na+
查看答案和解析>>
科目:高中化學 來源:2016-2017學年安徽師大附中高二上10月月考化學卷(解析版) 題型:填空題
請根據所學知識回答下列問題:
(1)同溫同壓下,反應H2(g)+Cl2(g)===2HCl(g)在光照和點燃條件下的ΔH(化學計量數相同)分別為ΔH1、ΔH2,ΔH1____________ΔH2(填“>”“<”或“=”下同)。
(2)相同條件下,2 mol氫原子所具有的能量____________1 mol 氫分子所具有的能量。
(3)已知:常溫下,0.01 mol·L-1 MOH溶液的pH為10,MOH(aq)與H2SO4(aq)反應生成1 mol可溶正鹽的ΔH=-24.2 kJ·mol-1,強酸與強堿的稀溶液的中和熱為ΔH=-57.3 kJ·mol-1。則MOH在水溶液中電離的ΔH為_______________
(4)土壤中的微生物可將大氣中H2S經兩步反應氧化成SO42-,兩步反應的能量變化示意圖如下:
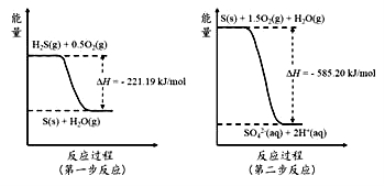
1mol H2S(g)全部氧化成SO42-(aq)的熱化學方程式為______________________。
(5)一定條件,在水溶液中1 mol Cl-、ClO x-(x=1,2,3,4)的能量(KJ)相對大小如圖所示。
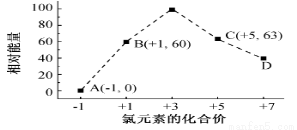
①D是______________________ (填離子符號)。
②B→A+C反應的熱化學方程式為______________________ (用離子符號表示)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com