
| A. | 在海輪外殼上鑲入鋅塊,可減緩船體的腐蝕速率 | |
| B. | 工業粉塵中含有Pb、Cd、Cr、V、As等金屬元素,過量攝入均對人體有害 | |
| C. | 用工業明膠制作用藥膠囊,會導致過量Cr元素攝入人體而提高致癌風險 | |
| D. | 分光光度計通過測定溶液顏色分析反應物(或生成物)濃度變化,從而確定化學反應速率 |
分析 A.利用原電池保護不活潑金屬;
B.As為非金屬元素;
C.Cr是重金屬元素,攝入過量使人體蛋白質變性;
D.由利用溶液顏色與反應物(或生成物)濃度的關系,可以確定該化學反應的速率,分光光度計可進行比色分析.
解答 解:A.在海輪外殼上鑲入鋅塊,形成原電池,鋅作負極失電子,輪船外殼鐵作正極被保護,可減緩船體的腐蝕速率,故A正確;
B.As為非金屬元素,故B錯誤;
C.Cr是重金屬元素,攝入過量使人體蛋白質變性,提高致癌風險,故C正確;
D.由利用溶液顏色與反應物(或生成物)濃度的關系,可以確定該化學反應的速率,分光光度計可進行比色分析,故D正確;
故選B.
點評 本題考查金屬的腐蝕與防護、物質的性質,平時多積累這些基礎知識,題目難度不大,注重化學與生活的聯系.


 智慧小復習系列答案
智慧小復習系列答案科目:高中化學 來源: 題型:選擇題
| A. | 鋁和氫氧化鈉溶液反應生成Al(OH)3和Na | |
| B. | 鈉在空氣中燃燒生成淡黃色的NaO2 | |
| C. | 鐵在高溫下與水蒸氣反應生成Fe3O4和H2 | |
| D. | 用碳酸鈉和氫氧化鈣反應制NaHCO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2SO2(g)+O2(g)$?_{500℃}^{V_{2}O_{5}}$2SO3(g)△H=-196.6kJ/mol,若2molSO2完全反應則放出熱量等于196.6kJ | |
| B. | “冰,水為之,而寒于水”說明相同質量的水和冰比較,冰的能量高 | |
| C. | 已知C(石墨)=C(金剛石)△H=+1.9kJ/mol,則從能量角度看金剛石比石墨穩定 | |
| D. | 氫氣的燃燒熱為285.8kJ/mol,則氫氣燃燒的熱化學方程式為2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
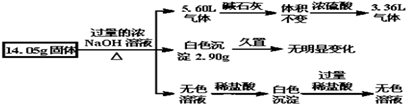
| A. | 一定含有Al,其物質的量為$\frac{5}{3}$mol | |
| B. | 一定不含FeCl2,可能含有MgCl2和AlCl3 | |
| C. | 一定含有(NH4)2SO4和FeCl2 | |
| D. | 一定含有(NH4)2SO4和MgCl2,且物質的量相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 實驗 | 操作 | |
| A | 觀察鈉與水反應的現象 | 用鑷子從煤油中取出金屬鈉,切下綠豆大小的鈉,小心放入裝滿水的燒杯中 |
| B | 檢驗NaHCO3與Na2CO3溶液 | 用小試管分別取少量溶液,然后滴加澄清石灰水 |
| C | 證明Na2O2與CO2是放熱反應 | Na2O2用棉花包裹,放入充滿CO2的集氣瓶中,棉花燃燒說明是放熱反應 |
| D | 檢驗Na2CO3與K2CO3溶液 | 用稀硫酸清洗過的鉑絲分別蘸取溶液,在酒精燈外焰上灼燒,透過藍色鈷玻璃觀察火焰的顏色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
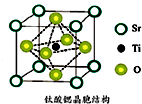 氫能被視作連接化石能源和可再生能源的重要橋梁.
氫能被視作連接化石能源和可再生能源的重要橋梁.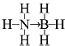 ;與氨硼烷互為等電子體的有機小分子是CH3CH3(寫結構簡式).
;與氨硼烷互為等電子體的有機小分子是CH3CH3(寫結構簡式).查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 7.8 g Na2O2中所含陰離子的數目是0.2NA | |
| B. | 標準狀況下,22.4 L SO3含分子數為NA | |
| C. | 標準狀況下,2.24 L 18O2中所含中子的數目是2NA | |
| D. | 用足量NaOH溶液完全吸收1 mol Cl2時,轉移電子的數目是2NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com