
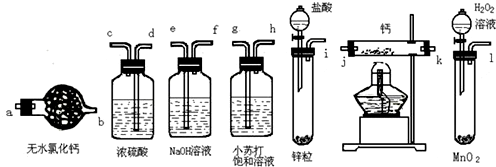
分析 (1)一般制備純凈干燥的氣體的實驗裝置的順序為:制備裝置→除雜裝置→干燥裝置等;
(2)實驗過程中要保證整個裝置內已充滿氫氣,實驗的操作程序是:檢查裝置的氣密性→產生氫氣→收集氫氣并進行驗純→加熱反應→停止加熱→繼續通氫氣至冷卻→停止通入氫氣;
(3)CaH2中H元素的化合價為-1價,CaH2具有還原性,與水發生氧化還原反應生成Ca(OH)2和H2;Ca與水反應也能產生Ca(OH)2和H2.
解答 解:(1)鈣屬于極活潑的金屬,極易與水反應生成氫氧化鈣和氫氣,而制備的氫氣中會混有水蒸氣和氯化氫,所以在與鈣化合之前需要除雜和干燥,分別選用試劑是氫氧化鈉和濃硫酸;同時為防止空氣中水蒸氣進入,最后還需要連接干燥管,所以正確的順序為:ief ab j k(或k,j)d;
故答案為:ief ab j k(或k,j)d;
(2)由于多余的氫氣需要燃燒反應掉,所以應該先收集一部分氣體并檢驗其純度,反應結束后還需要使氫化鈣在氫氣的氛圍中冷卻,所以應該最后關閉分液漏斗活塞,因此正確的順序為BADC,
故答案為:BADC;
(3)CaH2和Ca與水反應都能產生Ca(OH)2和H2,反應方程式分別為:CaH2+2H2O=Ca(OH)2+2H2↑和Ca+2H2O=Ca(OH)2+H2↑,因此不能根據反應后溶液呈堿性判斷是否含有CaH2,
故答案為:CaH2+2H2O=Ca(OH)2+2H2↑;Ca+2H2O═Ca(OH)2+H2↑.
點評 本題考查元素化合物知識,涉及到物質的性質和制備實驗,注意實驗的一般方法來解答,題目難度不大.


 黃岡小狀元口算速算練習冊系列答案
黃岡小狀元口算速算練習冊系列答案 成功訓練計劃系列答案
成功訓練計劃系列答案 倍速訓練法直通中考考點系列答案
倍速訓練法直通中考考點系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作業本系列答案
名校作業本系列答案科目:高中化學 來源: 題型:選擇題
| A. | 由石墨制備金剛石是吸熱反應;等質量時,石墨的能量比金剛石的低 | |
| B. | 由石墨制備金剛石是吸熱反應;等質量時,石墨的能量比金剛石的高 | |
| C. | 由石墨制備金剛石是放熱反應;等質量時,石墨的能量比金剛石的低 | |
| D. | 由石墨制備金剛石是放熱反應;等質量時,石墨的能量比金剛石的高 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 改變條件,反應物的轉化率增大,平衡常數也一定增大 | |
| B. | 反應2NO2(g)═N2O4(g)△H<0,升高溫度該反應平衡常數增大 | |
| C. | 對于給定可逆反應,溫度一定時,其正、逆反應的平衡常數相等 | |
| D. | 平衡常數為K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$的反應,化學方程式為CO2+H2$?_{加熱}^{催化劑}$CO+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3種 | B. | 4種 | C. | 5種 | D. | 6種 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Al在氧氣中生成Al2O3,Fe在氧氣中也生成Fe2O3 | |
| B. | 第VA族氫化物的熔沸點順序是NH3>AsH3>PH3;則第 VIA族氫化物的熔沸點順序也是H2O>H2Se>H2S | |
| C. | 工業上用電解熔融的氯化鎂制備鎂單質,工業上也可用電解熔融的氯化鋁制備鋁單質 | |
| D. | BaCl2溶液中通入SO2無沉淀產生,則Ba(NO3)2溶液中通入SO2也無沉淀產生 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com